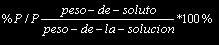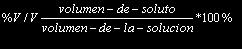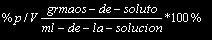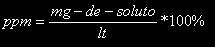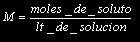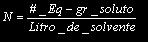EL AGUA Y LAS SOLUCIONES
Una solución (o disolución) es una mezcla de dos o más componentes, perfectamente homogénea ya que cada componente se mezcla íntimamente con el otro, de modo tal que pierden sus características individuales. Esto último significa que los constituyentes son indistinguibles y el conjunto se presenta en una sola fase (sólida, líquida o gas) bien definida.
Una solución que contiene agua como solvente se llama solución acuosa.
Si se analiza una muestra de alguna solución puede apreciarse que en cualquier parte de ella su composición es constante.
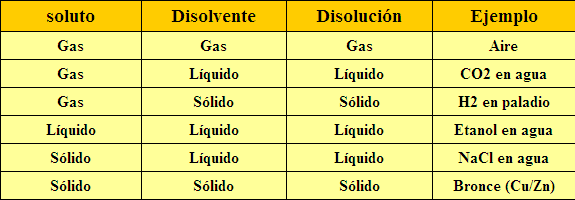
Entonces, reiterando, llamaremos solución o disolución a las mezclas homogéneas que se encuentran en fase líquida. Es decir, las mezclas homogéneas que se presentan en fase sólida, como las aleaciones (acero, bronce, latón) o las que se hallan en fase gaseosa (aire, humo, etc.) no se les conoce como disoluciones.
Las mezclas de gases, tales como la atmósfera, a veces también se consideran como soluciones.
Las soluciones son distintas de los coloides y de las suspensiones en que las partículas del soluto son de tamaño molecular y están dispersas uniformemente entre las moléculas del solvente.
Las sales, los ácidos, y las bases se ionizan cuando se disuelven en el agua
Características de las soluciones (o disoluciones):
I) Sus componente no pueden separarse por métodos físicos simples como decantación, filtración, centrifugación, etc.
II) Sus componentes sólo pueden separase por destilación, cristalización, cromatografía.
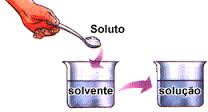
III) Los componentes de una solución son soluto y solvente.
Soluto: es aquel componente que se encuentra en menor cantidad y es el que se disuelve. El soluto puede ser sólido, líquido o gas, como ocurre en las bebidas gaseosas, donde el dióxido de carbono se utiliza como gasificante de las bebidas. El azúcar se puede utilizar como un soluto disuelto en líquidos (agua).
Solvente: es aquel componente que se encuentra en mayor cantidad y es el medio que disuelve al soluto. El solvente es aquella fase en que se encuentra la solución. Aunque un solvente puede ser un gas, líquido o sólido, el solvente más común es el agua.
IV) En una disolución, tanto el soluto como el solvente interactúan a nivel de sus componentes más pequeños (moléculas, iones). Esto explica el carácter homogéneo de las soluciones y la imposibilidad de separar sus componentes por métodos mecánicos.
Una solución que contiene agua como solvente se llama solución acuosa.
Si se analiza una muestra de alguna solución puede apreciarse que en cualquier parte de ella su composición es constante.
Entonces, reiterando, llamaremos solución o disolución a las mezclas homogéneas que se encuentran en fase líquida. Es decir, las mezclas homogéneas que se presentan en fase sólida, como las aleaciones (acero, bronce, latón) o las que se hallan en fase gaseosa (aire, humo, etc.) no se les conoce como disoluciones.
Las mezclas de gases, tales como la atmósfera, a veces también se consideran como soluciones.
Las soluciones son distintas de los coloides y de las suspensiones en que las partículas del soluto son de tamaño molecular y están dispersas uniformemente entre las moléculas del solvente.
Las sales, los ácidos, y las bases se ionizan cuando se disuelven en el agua
Características de las soluciones (o disoluciones):
I) Sus componente no pueden separarse por métodos físicos simples como decantación, filtración, centrifugación, etc.
II) Sus componentes sólo pueden separase por destilación, cristalización, cromatografía.
III) Los componentes de una solución son soluto y solvente.
Soluto: es aquel componente que se encuentra en menor cantidad y es el que se disuelve. El soluto puede ser sólido, líquido o gas, como ocurre en las bebidas gaseosas, donde el dióxido de carbono se utiliza como gasificante de las bebidas. El azúcar se puede utilizar como un soluto disuelto en líquidos (agua).
Solvente: es aquel componente que se encuentra en mayor cantidad y es el medio que disuelve al soluto. El solvente es aquella fase en que se encuentra la solución. Aunque un solvente puede ser un gas, líquido o sólido, el solvente más común es el agua.
IV) En una disolución, tanto el soluto como el solvente interactúan a nivel de sus componentes más pequeños (moléculas, iones). Esto explica el carácter homogéneo de las soluciones y la imposibilidad de separar sus componentes por métodos mecánicos.
CLASES DE SOLUCIONES Y FACTORES DE SOLUBILIDAD
SOLUBILIDAD
Es la cantidad máxima de un soluto que puede disolverse en una cantidad determinada de solvente a una temperatura previamente establecida. Generalmente, la solubilidad de una sustancia se expresa en gramos de soluto por cada 100 gramos de disolvente, por ejemplo a 20 ºC, la cantidad de cloruro de sodio que se puede disolver en 100 g de agua son 36 g; la máxima cantidad de nitrato de plata es 225 g y de permanganato de potasio es de 6,4 g.
Qué significa la siguiente expresión: a 50ºC la solubilidad del bromuro de potasio en 100 gramos de agua es 116 gramos
El término solubilidad ha de entenderse como la cantidad máxima de soluto en un solvente. Así, la expresión significa que al tomar 100 gramos de agua a 50 ºC en ella se disuelven exactamente 116 gramos de bromuro de potasio
Qué significa la expresión: la solubilidad del disolvente orgánico benceno en agua es de 0,22 gramos de soluto por cada 100 gramos de agua
La solubilidad es una propiedad característica de cada sustancia en un determinado solvente. Cualitativamente hablando, un soluto también se describe como insoluble, poco soluble y muy soluble en un solvente dado, para indicar muy aproximadamente la mayor o menor cantidad de soluto que se disuelve en una cantidad dada de este solvente.
EL PROCESO DE SOLUBILIDAD
Cuando un sólido iónico como bromuro de potasio se pone en contacto con el agua , los iones que lo forman se separan en ion potasio y anión cloruro.. Puesto que las moléculas del agua son polares, los cationes potasio son rodeados por los polos negativos del agua y los aniones cloruros son rodeados por los polos positivos. El proceso de orientación de las moléculas alrededor de los iones se llama hidratación..
Para que una sustancia se disuelva en agua, debe ser polar. Recuérdese que el enlace iónico es un extremo del enlace polar y cuando más polar sea una sustancia, más soluble es en agua . En química existe una regla de solubilidad: lo semejante disuelve lo semejante. Esto quiere decir que un solvente polar disuelve solutos polares y un solvente no polar disuelve solutos no polares .
El proceso de solubilidad frecuentemente esta asociado con absorción o emisión de calor. Por tanto, hay procesos de solubilidad exotérmicos y endotérmicos
FACTORES DE SOLUBILIDAD
El factor determinante de la solubilidad es la naturaleza del soluto y del solvente. Además de ello, la temperatura y la presión también influyen en la solubilidad de una sustancia
¨ TEMPERATURA
La temperatura afecta la rapidez y el grado de solubilidad. Al moverse las moléculas del solvente rápidamente, debido al aumento de temperatura, el soluto penetra más fácilmente y en mayor cantidad por entre las moléculas del solvente. Cuando el soluto es una gas, al aumentar la temperatura la solubilidad disminuye, ya que las moléculas del gases se escapan de la solución.
¨ LA PRESIÓN
El efecto de la variación de presión es prácticamente nulo sobre la solubilidad de sólidos y líquidos, pero es grande sobre la solubilidad de los gases. A mayor presión, mayor es la solubilidad de un gas.
Las gaseosas son embotelladas a alta presión. Por eso cuando se destapan, el gas que está disuelto sale produciendo burbujas.
El proceso de solubilidad de un sólido varía también con el tamaño de las partículas disueltas. Cuando más pequeñas sean éstas, mayor es la solubilidad. La agitación durante el proceso facilita la disolución: permite obtener más rápidamente una mezcla homogénea.
CÓMO PUEDEN SER LAS SOLUCIONES?
SOLUCION SATURADA
Se dice que una solución está saturada cuando a una temperatura determinada en una cantidad dada de solvente se tiene disuelta la máxima cantidad de soluto que se pueda disolver. Por ejemplo una solución de bromuro de potasio que tenga disueltos 116 g de KBr en 100 g de agua a 50 ºC es una solución saturada: cualquier exceso de KBr se deposita en el fondo del recipiente
SOLUCION INSATURADA
Cuando a una temperatura determinada en una cantidad dada de solvente se tiene disuelto menos soluto del que se puede disolver en ese solvente, se dice que la solución es insaturada.
En el caso del bromuro de potasio, si en lugar de tener exactamente 116 g en 100 g de agua, tenemos 90 g de KBr, la solución está insaturada.
SOLUCIONES SOBRESATURADAS
A pesar de que las concentraciones de una solución está limitada por la solubilidad máxima del soluto, es posible preparar soluciones que contengan disuelta una cantidad mayor de soluto a una temperatura T establecida. Estas soluciones se conocen como sobresaturadas. De esta manera, una solución de bromuro de sodio que contenga disueltos 116,5 g de la sustancia es una solución sobresaturada
La sobresaturación de una solución es un proceso muy cuidadoso, generalmente se realiza por calentamiento.
Mediante este proceso, parte del soluto por encima de la solubilidad máxima se disuelve. Al enfriar lentamente y en reposo la solución hasta la temperatura requerida, se obtiene la solución sobresaturada.
Estas soluciones precipitan soluto al agitarlas o al adicionarles una pequeña cantidad de soluto.
Es la cantidad máxima de un soluto que puede disolverse en una cantidad determinada de solvente a una temperatura previamente establecida. Generalmente, la solubilidad de una sustancia se expresa en gramos de soluto por cada 100 gramos de disolvente, por ejemplo a 20 ºC, la cantidad de cloruro de sodio que se puede disolver en 100 g de agua son 36 g; la máxima cantidad de nitrato de plata es 225 g y de permanganato de potasio es de 6,4 g.
Qué significa la siguiente expresión: a 50ºC la solubilidad del bromuro de potasio en 100 gramos de agua es 116 gramos
El término solubilidad ha de entenderse como la cantidad máxima de soluto en un solvente. Así, la expresión significa que al tomar 100 gramos de agua a 50 ºC en ella se disuelven exactamente 116 gramos de bromuro de potasio
Qué significa la expresión: la solubilidad del disolvente orgánico benceno en agua es de 0,22 gramos de soluto por cada 100 gramos de agua
La solubilidad es una propiedad característica de cada sustancia en un determinado solvente. Cualitativamente hablando, un soluto también se describe como insoluble, poco soluble y muy soluble en un solvente dado, para indicar muy aproximadamente la mayor o menor cantidad de soluto que se disuelve en una cantidad dada de este solvente.
EL PROCESO DE SOLUBILIDAD
Cuando un sólido iónico como bromuro de potasio se pone en contacto con el agua , los iones que lo forman se separan en ion potasio y anión cloruro.. Puesto que las moléculas del agua son polares, los cationes potasio son rodeados por los polos negativos del agua y los aniones cloruros son rodeados por los polos positivos. El proceso de orientación de las moléculas alrededor de los iones se llama hidratación..
Para que una sustancia se disuelva en agua, debe ser polar. Recuérdese que el enlace iónico es un extremo del enlace polar y cuando más polar sea una sustancia, más soluble es en agua . En química existe una regla de solubilidad: lo semejante disuelve lo semejante. Esto quiere decir que un solvente polar disuelve solutos polares y un solvente no polar disuelve solutos no polares .
El proceso de solubilidad frecuentemente esta asociado con absorción o emisión de calor. Por tanto, hay procesos de solubilidad exotérmicos y endotérmicos
FACTORES DE SOLUBILIDAD
El factor determinante de la solubilidad es la naturaleza del soluto y del solvente. Además de ello, la temperatura y la presión también influyen en la solubilidad de una sustancia
¨ TEMPERATURA
La temperatura afecta la rapidez y el grado de solubilidad. Al moverse las moléculas del solvente rápidamente, debido al aumento de temperatura, el soluto penetra más fácilmente y en mayor cantidad por entre las moléculas del solvente. Cuando el soluto es una gas, al aumentar la temperatura la solubilidad disminuye, ya que las moléculas del gases se escapan de la solución.
¨ LA PRESIÓN
El efecto de la variación de presión es prácticamente nulo sobre la solubilidad de sólidos y líquidos, pero es grande sobre la solubilidad de los gases. A mayor presión, mayor es la solubilidad de un gas.
Las gaseosas son embotelladas a alta presión. Por eso cuando se destapan, el gas que está disuelto sale produciendo burbujas.
El proceso de solubilidad de un sólido varía también con el tamaño de las partículas disueltas. Cuando más pequeñas sean éstas, mayor es la solubilidad. La agitación durante el proceso facilita la disolución: permite obtener más rápidamente una mezcla homogénea.
CÓMO PUEDEN SER LAS SOLUCIONES?
SOLUCION SATURADA
Se dice que una solución está saturada cuando a una temperatura determinada en una cantidad dada de solvente se tiene disuelta la máxima cantidad de soluto que se pueda disolver. Por ejemplo una solución de bromuro de potasio que tenga disueltos 116 g de KBr en 100 g de agua a 50 ºC es una solución saturada: cualquier exceso de KBr se deposita en el fondo del recipiente
SOLUCION INSATURADA
Cuando a una temperatura determinada en una cantidad dada de solvente se tiene disuelto menos soluto del que se puede disolver en ese solvente, se dice que la solución es insaturada.
En el caso del bromuro de potasio, si en lugar de tener exactamente 116 g en 100 g de agua, tenemos 90 g de KBr, la solución está insaturada.
SOLUCIONES SOBRESATURADAS
A pesar de que las concentraciones de una solución está limitada por la solubilidad máxima del soluto, es posible preparar soluciones que contengan disuelta una cantidad mayor de soluto a una temperatura T establecida. Estas soluciones se conocen como sobresaturadas. De esta manera, una solución de bromuro de sodio que contenga disueltos 116,5 g de la sustancia es una solución sobresaturada
La sobresaturación de una solución es un proceso muy cuidadoso, generalmente se realiza por calentamiento.
Mediante este proceso, parte del soluto por encima de la solubilidad máxima se disuelve. Al enfriar lentamente y en reposo la solución hasta la temperatura requerida, se obtiene la solución sobresaturada.
Estas soluciones precipitan soluto al agitarlas o al adicionarles una pequeña cantidad de soluto.
DEFINICIÓN DE CONCENTRACIÓN
La concentración de una solución expresa la cantidad de soluto presente en una cantidad dad de solvente o de solución. En términos cuantitativos, esto es, la relación o proporción matemática entre la cantidad de soluto y la cantidad de solvente o, entre soluto y solución. Esta relación suele expresarse en porcentaje.
UNIDADES DE CONCENTRACIÓN
Unidades Físicas
Porcentaje referido a la masa: Relaciona la masa del soluto, en gramos, presente en una cantidad dad de solución. Teniendo en cuenta que el resultado se expresa como porcentaje de soluto, la cantidad de patrón de solución suele tomar como 100 gr.
Porcentaje referido al volumen: Se refiere al volumen de soluto, en mL, presente en cada 100 ml de solución La expresión que utilizamos para calcularlo es:
Porcentaje masa volumen: Representa la masa de soluto (en gr) por cada 100 ml de solución. Se puede calcular según la expresión:
Partes por millón (ppm)Para medir algunas concentraciones pequeñas, por ejemplo, las partículas contaminantes que eliminan los automotores o la cantidad de cloro o fluor presentes en el agua potable, se utiliza una unidad de concentración denominada partes por millón (ppm), que mide las partes de soluto presentes en un millón de partes de solución. Para soluciones solidad se utilizan, por lo general, las unidades mg/Kg. y las soluciones liquidas mg/L. La siguiente expresión, permite calcular las partes por millón:
Unidades Quimicas
Molaridad (M): Es la forma más usual de expresar la concentración de una solución. Se define como el numero de moles de soluto disueltos en un litro de solución. Alternativamente, se puede expresar como mili moles de soluto disuelto en mL de solución. Matemáticamente se expresa así:
Molalidad (m): Indica la cantidad de moles de soluto presentes en un Kg. (1.000 gr) de solvente. Cuando el solvente de agua, y debido a que la densidad de esta es 1gr/ml, 1 Kg. de agua equivalente a un litro. La molalidad se calcula mediante la expresión:
Normalidad (N): Relaciona el numeró de equivalentes gramos o equivalentes químicos de un soluto con la cantidad de solución, en litros. Se expresa como:
El concepto de equivalente gramo o equivalente químico ha sido desarrollado especialmente para referirse a ácidos y bases. Así, un equivalente –gramo es la masa de sustancia (ácido _base) capaz de reproducir un mol de iones H+ o OH- , según el caso. Para pasar de moles a gramos se emplean las masas moleculares de las sustancias involucradas Dado que un ácido y una base reaccionan, a través de la neutralización mutua de los iones H+ o OH-, para producir las sales correspondientes y agua; el concepto de equivalente también se aplica para sales.
Fracción Molar (X): Expresa el número de moles de un componente de la solución, en relación con el número total de moles, incluyendo todos los componentes presentes calcula mediante la expresión:
DILUCIONES
Los reactivos disponibles en el laboratorio se encuentran, por lo general, en forma de sólidos o en soluciones comerciales muy concentradas (cercanas al 100%). Con cierta frecuencia, es necesario preparar soluciones menos concentradas, a partir de estos materiales, para lo cual debemos diluirlas (figura 15). Al diluir el volumen del solvente, aumenta el de la solución, mientras que el número total de moles o de moléculas del soluto permanece igual. Esto significa, que el número de moléculas o de moles del soluto al principio y al final, es el mismo. Lo más común es que las concentraciones de las sustancias se encuentren expresadas como molaridad. Si partimos de una solución inicial n1 :M1 .V1, para obtener una segunda solución n2 :M2 .V2, debe cumplirse que el número inicial de moles sea igual al número final de moles (n1 :n2). De ahí deducimos que
M1 .V1 :M2 .V2. Esta expresión es la clave para determinar el volumen final, V2, o la concentración final, M2, según sea el caso.
Cuando la concentración de la solución se expresa como normalidad, podemos basarnos en una generalización de la expresión anterior: C1 .V1 :C2 .V2, en donde C indica la concentración de la solución.
M1 .V1 :M2 .V2. Esta expresión es la clave para determinar el volumen final, V2, o la concentración final, M2, según sea el caso.
Cuando la concentración de la solución se expresa como normalidad, podemos basarnos en una generalización de la expresión anterior: C1 .V1 :C2 .V2, en donde C indica la concentración de la solución.
Propiedades coligativas de las soluciones y de los coloides
Cuando dos o más sustancias se mezclan para dar lugar a una solución, el resultado es una sustancia con una serie de propiedades físicas propias y diferentes a aquellas que poseían las sustancias originales. Estas propiedades emergentes en las soluciones reciben el nombre de propiedades coligativas y dependen directamente de la concentración de soluto, mas no de su naturaleza química. A continuación profundizaremos sobre algunas de estas propiedades.
PRESIÓN DE VAPOR
Las moléculas de un líquido cualquiera, a una determinada temperatura, poseen una cierta cantidad de energía cinética. Algunas moléculas, especialmente aquellas situadas cerca de la superficie, pasan espontáneamente al estado gaseoso, es decir, se volatilizan. No obstante, como resultado de las constantes colisiones entre moléculas, muchas de estas regresan nuevamente al líquido, dando como resultado un estado de equilibrio entre las fases gaseosa y líquida de la sustancia. Ahora bien, si el líquido se halla contenido en un recipiente cerrado, la fracción gaseosa ejercerá presión sobre la tapa del recipiente, al golpearla continuamente. Esta presión, denominada presión de vapor, se puede medir y es característica de cada sustancia.
La proporción entre las fases gas-líquido, depende de la fuerza de cohesión existente entre las moléculas. Si la cohesión es débil, una gran cantidad de moléculas se volatilizarán. Mientras que, si la cohesión es fuerte, serán muy pocas las que lo consigan. Esto es lo que determina que unas sustancias sean más volátiles que otras. Por otro lado, la presión de vapor aumenta con la temperatura, ya que, al contar con mayor energía cinética, más moléculas pasarán a la fase gaseosa.
Una solución cuyo soluto sea no volátil, poseerá una presión de vapor menor que la observada en el solvente puro. Por el contrario, si el soluto es volátil, la presión de vapor de la solución será la suma de las presiones parciales de los componentes de la mezcla. Estas relaciones se resumen en la ley de Raoult, formulada por François Raoult(1830-1901) en 1887.
Matemáticamente, la ley de Raoult se expresa así cuando el soluto es no volátil:
PA :Po A .XA
Donde PA es la presión de vapor de la solución, PAoes la presión de vapor del solvente puro y XA es la fracción molar del solvente en la solución. Así, entre más diluida sea la solución, menor será la disminución de la presión de vapor.
Para dos componentes volátiles tendremos:
Psolución:PA +PB,
donde Psolución es la presión de vapor de la solución final, y PA y PB representan las presiones parciales de los componentes A y B, calculadas según la fórmula anterior.
Las moléculas de un líquido cualquiera, a una determinada temperatura, poseen una cierta cantidad de energía cinética. Algunas moléculas, especialmente aquellas situadas cerca de la superficie, pasan espontáneamente al estado gaseoso, es decir, se volatilizan. No obstante, como resultado de las constantes colisiones entre moléculas, muchas de estas regresan nuevamente al líquido, dando como resultado un estado de equilibrio entre las fases gaseosa y líquida de la sustancia. Ahora bien, si el líquido se halla contenido en un recipiente cerrado, la fracción gaseosa ejercerá presión sobre la tapa del recipiente, al golpearla continuamente. Esta presión, denominada presión de vapor, se puede medir y es característica de cada sustancia.
La proporción entre las fases gas-líquido, depende de la fuerza de cohesión existente entre las moléculas. Si la cohesión es débil, una gran cantidad de moléculas se volatilizarán. Mientras que, si la cohesión es fuerte, serán muy pocas las que lo consigan. Esto es lo que determina que unas sustancias sean más volátiles que otras. Por otro lado, la presión de vapor aumenta con la temperatura, ya que, al contar con mayor energía cinética, más moléculas pasarán a la fase gaseosa.
Una solución cuyo soluto sea no volátil, poseerá una presión de vapor menor que la observada en el solvente puro. Por el contrario, si el soluto es volátil, la presión de vapor de la solución será la suma de las presiones parciales de los componentes de la mezcla. Estas relaciones se resumen en la ley de Raoult, formulada por François Raoult(1830-1901) en 1887.
Matemáticamente, la ley de Raoult se expresa así cuando el soluto es no volátil:
PA :Po A .XA
Donde PA es la presión de vapor de la solución, PAoes la presión de vapor del solvente puro y XA es la fracción molar del solvente en la solución. Así, entre más diluida sea la solución, menor será la disminución de la presión de vapor.
Para dos componentes volátiles tendremos:
Psolución:PA +PB,
donde Psolución es la presión de vapor de la solución final, y PA y PB representan las presiones parciales de los componentes A y B, calculadas según la fórmula anterior.
PUNTO DE EBULLICIÓN
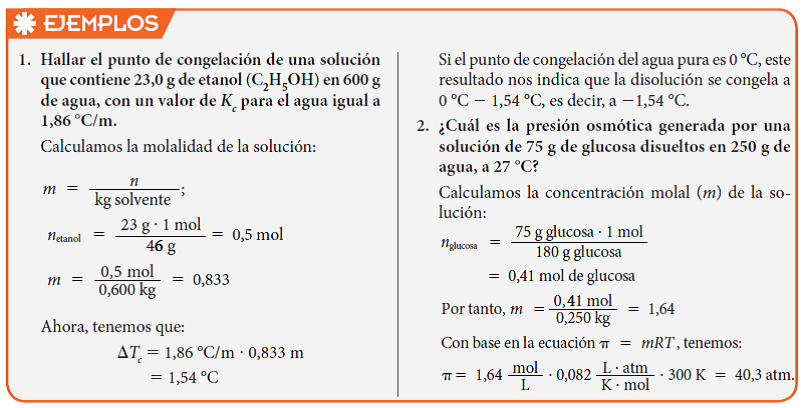
El punto de ebullición de un líquido es la temperatura a la cual su presión de vapor es igual a la presión atmosférica. Si a este líquido se le adiciona un soluto no volátil, la temperatura de ebullición de la solución resultante, aumenta. Experimentalmente se ha encontrado que la elevación del punto de ebullición DTees proporcional a la concentración molal (m) de la solución, según la expresión: DTe:Ke.m
Donde, m es la concentración molal y Kees la constante de proporcionalidad,llamada constante ebulloscópica molal. Kese expresa en °C/m y es característica de cada solvente.
El punto de ebullición de un líquido es la temperatura a la cual su presión de vapor es igual a la presión atmosférica. Si a este líquido se le adiciona un soluto no volátil, la temperatura de ebullición de la solución resultante, aumenta. Experimentalmente se ha encontrado que la elevación del punto de ebullición DTees proporcional a la concentración molal (m) de la solución, según la expresión: DTe:Ke.m
Donde, m es la concentración molal y Kees la constante de proporcionalidad,llamada constante ebulloscópica molal. Kese expresa en °C/m y es característica de cada solvente.
PUNTO DE CONGELACIÓN
En soluciones formadas por solutos no volátiles se observa un descenso de la temperatura de congelación, respecto a la del solvente puro. Esta disminución es proporcional a la concentración molal de la solución y se relaciona por medio de la constante crioscópica molal, que se expresa en °C/m y depende de la naturaleza del solvente. La expresión matemática es:
DTc:Kc .m
Una de las aplicaciones de esta propiedad coligativa se relaciona con los anticongelantes, sustancias empleadas principalmente en automóviles para evitar que el agua de los radiadores se congele durante el invierno.
En soluciones formadas por solutos no volátiles se observa un descenso de la temperatura de congelación, respecto a la del solvente puro. Esta disminución es proporcional a la concentración molal de la solución y se relaciona por medio de la constante crioscópica molal, que se expresa en °C/m y depende de la naturaleza del solvente. La expresión matemática es:
DTc:Kc .m
Una de las aplicaciones de esta propiedad coligativa se relaciona con los anticongelantes, sustancias empleadas principalmente en automóviles para evitar que el agua de los radiadores se congele durante el invierno.
PRESIÓN OSMÓTICA
La ósmosis es un fenómeno que se aplica especialmente a soluciones en las cuales el solvente es el agua. Consiste en el paso de moléculas de agua (solvente) a través de una membrana semipermeable, desde un compartimiento menos concentrado hacia otro, con mayor concentración de soluto.
Una membrana semipermeable es una película, que permite el paso del solvente más no del soluto. Las moléculas del solvente pueden pasar en ambas direcciones, a través de la membrana, pero el flujo predominante ocurre en la dirección menor a mayor concentración de soluto y termina cuando la presión ejercida por el golpeteo de moléculas de soluto a uno y otro lado de la membrana, se iguala. Este golpeteo se traduce en un valor de presión, ejercida por las moléculas de soluto sobre la membrana, denominada presión osmótica. La presión osmótica depende de la cantidad de soluto y puede interpretarse como si el soluto fuera un gas que ejerce presión sobre las paredes de un recipiente, su expresión matemática es:
Π:nRT
V
donde, π representa la presión osmótica, n/V se interpreta como la concentración molar de la solución y R es la constante universal de los gases. Si el solvente es agua, la molaridad será equivalente a la molalidad. De donde,obtenemos que:
π :MRT :mRT
La ósmosis es un fenómeno que se aplica especialmente a soluciones en las cuales el solvente es el agua. Consiste en el paso de moléculas de agua (solvente) a través de una membrana semipermeable, desde un compartimiento menos concentrado hacia otro, con mayor concentración de soluto.
Una membrana semipermeable es una película, que permite el paso del solvente más no del soluto. Las moléculas del solvente pueden pasar en ambas direcciones, a través de la membrana, pero el flujo predominante ocurre en la dirección menor a mayor concentración de soluto y termina cuando la presión ejercida por el golpeteo de moléculas de soluto a uno y otro lado de la membrana, se iguala. Este golpeteo se traduce en un valor de presión, ejercida por las moléculas de soluto sobre la membrana, denominada presión osmótica. La presión osmótica depende de la cantidad de soluto y puede interpretarse como si el soluto fuera un gas que ejerce presión sobre las paredes de un recipiente, su expresión matemática es:
Π:nRT
V
donde, π representa la presión osmótica, n/V se interpreta como la concentración molar de la solución y R es la constante universal de los gases. Si el solvente es agua, la molaridad será equivalente a la molalidad. De donde,obtenemos que:
π :MRT :mRT
COLOIDES
Los coloides son un estado intermedio entre mezclas homogéneas o verdaderas soluciones y mezclas heterogéneas. El factor determinante en esta diferenciación es el tamaño de las partículas disueltas (solutos).
CARACTERÍSTICAS DE LOS COLOIDES
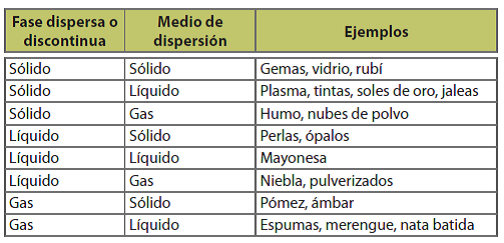
En las soluciones el soluto presenta moléculas pequeñas, imposibles de filtrar o de separar por medios físicos. Por el contrario, en mezclas heterogéneas es posible distinguir cada uno de los componentes y separarlos físicamente. En los coloides, el tamaño del soluto es tal, que sus partículas se encuentran suspendidas entre aquellas del solvente, sin alcanzar a precipitarse, pero siendo lo suficientemente grandes como para causar turbidez en la mezcla. Así, en un coloide es posible identificar una fase dispersa (soluto) y una fase dispersante (solvente). A continuación se muestran algunos ejemplos de soluciones coloidales:
PROPIEDADES DE LOS COLOIDES
Los coloides presentan las siguientes propiedades:
· Movimiento browniano
En una solución verdadera las moléculas están siempre en rápido movimiento.
Tanto las moléculas de soluto como las de solvente presentan movimiento molecular. Como las partículas coloidales son grandes, por lo general formadas por agregados moleculares, su movimiento es más lento. Aparentemente la causa del movimiento de las partículas coloidales es el bombardeo que reciben de las moléculas del medio en el cual están dispersas. Robert Brown (1773–1858) fue el primero que observó, en el ultramicroscopio, este movimiento errático, llamado en su honor movimiento browniano. Este movimiento es una de las razones por las que las partículas coloidales no se sedimentan, a pesar de su gran tamaño, aun cuando se dejen en reposo por un tiempo prolongado.
· Efecto Tyndall
Cuando un haz de luz pasa a través de un coloide, las partículas dispersas difractan la luz, haciendo que se forme un rayo de luz angosto, dentro del cual es posible observar pequeñas manchas luminosas, que corresponden a la luz reflejada sobre la superficie de las partículas coloidales.
Esto no ocurre en soluciones verdaderas, pues las partículas de soluto son demasiado pequeñas como para desviar la luz. Este fenómeno recibe el nombre de efecto Tyndall, en honor a su descubridor.
· Adsorción
La adsorción es la retención de las moléculas constitutivas de una sustancia, sobre la superficie de otras moléculas, que actúan como adsorbentes.
Las partículas coloidales suelen ser excelentes adsorbentes, propiedad que tiene numerosas aplicaciones prácticas. Por ejemplo, el gel de sílice es un muy buen adsorbente frente a varias sustancias, especialmente el vapor de agua. Por esta razón, en el laboratorio y en la industria, el gel de sílice se emplea como agente desecante.
La adsorción se puede presentar en sustancias no coloidales como el carbón, que se emplea en las máscaras antigás para adsorber gases venenosos y en forma de pastillas para ayudar al tratamiento de indigestiones o como antídoto de primera urgencia en el tratamiento de ingestión de venenos.
En los laboratorios de química se emplea a menudo carbón en polvo para eliminar impurezas, por ejemplo, cuando se desea aislar y purificar un compuesto. También se pueden preparar columnas de un adsorbente como el óxido de aluminio, para separar materiales que se pueden adsorber a distintas alturas de la columna. Este procedimiento es la base del análisis cromatográfico de adsorción en columna.
· Carga eléctrica
Las partículas coloidales pueden poseer una carga eléctrica característica sobre su superficie. Esta carga puede ser el resultado de la adsorción de iones, el efecto de electricidad estática o la ionización de las propias partículas coloidales. El proceso responsable de la generación de la carga, determinará el signo de la misma. Dado que partículas de la misma carga se repelen, cuando las partículas coloidales tienen carga no forman agregados mayores, con lo cual se evita que precipiten en forma de coágulos, proceso denominado coagulación.
Esta propiedad se usa, entre otras aplicaciones, para separar los solutos constitutivos de un coloide. Por ejemplo, es frecuente tener sistemas coloidales formados por una mezcla de diferentes proteínas. Las proteínas son macromoléculas, que dependiendo del medio dispersante, se ionizan diferencialmente. El procedimiento se denomina electroforesis y consiste en someter la mezcla a la acción de un flujo eléctrico entre dos electrodos, de manera que las moléculas con carga negativa migran al ánodo (polo positivo), al tiempo que las cargadas positivamente se movilizan hacia el cátodo (polo negativo).
La electrofóresis es un procedimiento muy usado en la actualidad, por ejemplo, para separar las proteínas del plasma sanguíneo o para separar moléculas de ADN de origen diferente.
· Diálisis
Las sustancias que se disuelven formando soluciones verdaderas se llaman a veces cristaloides para diferenciarlas de los coloides. Los cristaloidespasan con facilidad a través de membranas que retienen a las partículas coloidales. Estas membranas se pueden considerar tamices con agujeros de un tamaño definido. La membrana se llama membranadializadora y el proceso de separación se llama diálisis. La mayoría de las membranas animales se pueden considerar membranas dializadoras.
· Movimiento browniano
En una solución verdadera las moléculas están siempre en rápido movimiento.
Tanto las moléculas de soluto como las de solvente presentan movimiento molecular. Como las partículas coloidales son grandes, por lo general formadas por agregados moleculares, su movimiento es más lento. Aparentemente la causa del movimiento de las partículas coloidales es el bombardeo que reciben de las moléculas del medio en el cual están dispersas. Robert Brown (1773–1858) fue el primero que observó, en el ultramicroscopio, este movimiento errático, llamado en su honor movimiento browniano. Este movimiento es una de las razones por las que las partículas coloidales no se sedimentan, a pesar de su gran tamaño, aun cuando se dejen en reposo por un tiempo prolongado.
· Efecto Tyndall
Cuando un haz de luz pasa a través de un coloide, las partículas dispersas difractan la luz, haciendo que se forme un rayo de luz angosto, dentro del cual es posible observar pequeñas manchas luminosas, que corresponden a la luz reflejada sobre la superficie de las partículas coloidales.
Esto no ocurre en soluciones verdaderas, pues las partículas de soluto son demasiado pequeñas como para desviar la luz. Este fenómeno recibe el nombre de efecto Tyndall, en honor a su descubridor.
· Adsorción
La adsorción es la retención de las moléculas constitutivas de una sustancia, sobre la superficie de otras moléculas, que actúan como adsorbentes.
Las partículas coloidales suelen ser excelentes adsorbentes, propiedad que tiene numerosas aplicaciones prácticas. Por ejemplo, el gel de sílice es un muy buen adsorbente frente a varias sustancias, especialmente el vapor de agua. Por esta razón, en el laboratorio y en la industria, el gel de sílice se emplea como agente desecante.
La adsorción se puede presentar en sustancias no coloidales como el carbón, que se emplea en las máscaras antigás para adsorber gases venenosos y en forma de pastillas para ayudar al tratamiento de indigestiones o como antídoto de primera urgencia en el tratamiento de ingestión de venenos.
En los laboratorios de química se emplea a menudo carbón en polvo para eliminar impurezas, por ejemplo, cuando se desea aislar y purificar un compuesto. También se pueden preparar columnas de un adsorbente como el óxido de aluminio, para separar materiales que se pueden adsorber a distintas alturas de la columna. Este procedimiento es la base del análisis cromatográfico de adsorción en columna.
· Carga eléctrica
Las partículas coloidales pueden poseer una carga eléctrica característica sobre su superficie. Esta carga puede ser el resultado de la adsorción de iones, el efecto de electricidad estática o la ionización de las propias partículas coloidales. El proceso responsable de la generación de la carga, determinará el signo de la misma. Dado que partículas de la misma carga se repelen, cuando las partículas coloidales tienen carga no forman agregados mayores, con lo cual se evita que precipiten en forma de coágulos, proceso denominado coagulación.
Esta propiedad se usa, entre otras aplicaciones, para separar los solutos constitutivos de un coloide. Por ejemplo, es frecuente tener sistemas coloidales formados por una mezcla de diferentes proteínas. Las proteínas son macromoléculas, que dependiendo del medio dispersante, se ionizan diferencialmente. El procedimiento se denomina electroforesis y consiste en someter la mezcla a la acción de un flujo eléctrico entre dos electrodos, de manera que las moléculas con carga negativa migran al ánodo (polo positivo), al tiempo que las cargadas positivamente se movilizan hacia el cátodo (polo negativo).
La electrofóresis es un procedimiento muy usado en la actualidad, por ejemplo, para separar las proteínas del plasma sanguíneo o para separar moléculas de ADN de origen diferente.
· Diálisis
Las sustancias que se disuelven formando soluciones verdaderas se llaman a veces cristaloides para diferenciarlas de los coloides. Los cristaloidespasan con facilidad a través de membranas que retienen a las partículas coloidales. Estas membranas se pueden considerar tamices con agujeros de un tamaño definido. La membrana se llama membranadializadora y el proceso de separación se llama diálisis. La mayoría de las membranas animales se pueden considerar membranas dializadoras.
| soluciones.pdf | |
| File Size: | 42 kb |
| File Type: | |
| soluciones_unidades_de_concentracion.pdf | |
| File Size: | 73 kb |
| File Type: | |
| propiedades_coligativas_de_soluciones.pdf | |
| File Size: | 259 kb |
| File Type: | |