VELOCIDAD DE REACCIÓN
En una reacción química, además de conocer los compuestos que intervienen,
es importante saber qué tan rápido reaccionan y los factores que determinan
esta velocidad. Así, es posible modificar o alterar el curso de la reacción para
buscar mayor eficiencia.
En una reacción química, además de conocer los compuestos que intervienen,
es importante saber qué tan rápido reaccionan y los factores que determinan
esta velocidad. Así, es posible modificar o alterar el curso de la reacción para
buscar mayor eficiencia.
Conceptos básicos
La velocidad de una reacción es la rapidez con la que se forman los productos o se consumen los reactivos involucrados en dicha reacción.
La velocidad de reacción se define en términos del tiempo necesario para que desaparezca o se transforme una determinada cantidad de reactivos o para que se formen los productos correspondientes. Decimos entonces que:
Velocidad : cambio en la concentración de una Sustancia consumida o formada
tiempo transcurrido
Consideremos una reacción cualquiera:
A2(g) B2(g) 2AB(g)
A medida que la reacción ocurre, las concentraciones de A2 y B2, disminuyen gradualmente, mientras que la concentración del producto, AB, aumenta en la misma proporción.
La velocidad de reacción para las especies A2 y B2 se puede expresar en términos del aumento en la concentración de AB, en un intervalo de tiempo:
Velocidad de reacción = AB
t
También podemos expresar la velocidad a partir de la tasa de descomposición de cualquiera de los dos reactivos:
Velocidad de reacción = A2 = B2
t t
La diferencia está en que en el caso de los productos hablamos de velocidad de formación, mientras que en el segundo caso se trata de velocidad de descomposición.
Observa que los corchetes se emplean para representar la concentración de una sustancia, como mol/litro. De donde, deducimos que las unidades en las que se expresa la velocidad son mol/litro/s
La velocidad de las reacciones químicas es una función de la concentración de las sustancias reaccionantes, pues se intuye que entre más moléculas de cada sustancia se tengan, mayor será la probabilidad de que entren en contacto unas con otras y por tanto, mayor será la rapidez con la que unas se transforman en otras.
La velocidad de una reacción es la rapidez con la que se forman los productos o se consumen los reactivos involucrados en dicha reacción.
La velocidad de reacción se define en términos del tiempo necesario para que desaparezca o se transforme una determinada cantidad de reactivos o para que se formen los productos correspondientes. Decimos entonces que:
Velocidad : cambio en la concentración de una Sustancia consumida o formada
tiempo transcurrido
Consideremos una reacción cualquiera:
A2(g) B2(g) 2AB(g)
A medida que la reacción ocurre, las concentraciones de A2 y B2, disminuyen gradualmente, mientras que la concentración del producto, AB, aumenta en la misma proporción.
La velocidad de reacción para las especies A2 y B2 se puede expresar en términos del aumento en la concentración de AB, en un intervalo de tiempo:
Velocidad de reacción = AB
t
También podemos expresar la velocidad a partir de la tasa de descomposición de cualquiera de los dos reactivos:
Velocidad de reacción = A2 = B2
t t
La diferencia está en que en el caso de los productos hablamos de velocidad de formación, mientras que en el segundo caso se trata de velocidad de descomposición.
Observa que los corchetes se emplean para representar la concentración de una sustancia, como mol/litro. De donde, deducimos que las unidades en las que se expresa la velocidad son mol/litro/s
La velocidad de las reacciones químicas es una función de la concentración de las sustancias reaccionantes, pues se intuye que entre más moléculas de cada sustancia se tengan, mayor será la probabilidad de que entren en contacto unas con otras y por tanto, mayor será la rapidez con la que unas se transforman en otras.
Teoría de las colisiones
Como se mencionó antes, una reacción química implica una reorganización espacial de los átomos en la ruptura, y posterior formación de enlaces químicos. Para que esto suceda, las moléculas y átomos involucrados, deben estar en contacto físico. Las particularidades del proceso de interacción entre sustancias químicas a nivel molecular se explican a partir de la teoría de las colisiones.
La teoría cinético-molecular de la materia nos dice que los átomos y moléculas de las distintas sustancias se hallan en continuo movimiento, lo que ocasiona choques constantes entre las partículas.
Estos choques son la chispa necesaria para que haya una reacción química. Así, mientras mayor sea el número de choques por unidad de tiempo, mayor será la probabilidad de que ocurra una reacción.
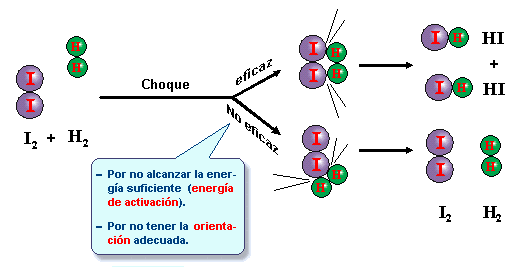
Sin embargo, no todos los choques son efectivos, en el sentido de que provoquen un cambio químico. Para que esto ocurra, las partículas en cuestión deben tener una energía suficientemente alta para vencer las fuerzas de repulsión que actúan entre ellas. De no ser así, dichas partículas se volverían a separar. Por otra parte, debido a que las moléculas suelen tener una compleja estructura tridimensional, alrededor de la cual se distribuyen nubes de electrones, los choques efectivos deben darse en una cierta orientación espacial. En otras palabras, la posición y la dirección con la cual se acerquen las moléculas determinará que se produzca o no una reacción (figura 3).
La energía necesaria para que sea posible una reacción se denomina energía de activación (Ea). La energía de activación es una propiedad de cada reacción y depende de la clase de enlaces que se tengan que romper durante la misma.
De lo anterior se concluye que la velocidad de reacción depende del número de choques por segundo, del número de choques efectivos, de la orientación con la cual ocurren los choques, de la energía que posean las moléculas en el momento de la colisión y de cuánta energía hace falta para alcanzar el valor crítico o energía de activación.
De ahí que, cualquier circunstancia que afecte la frecuencia y la efectividad de las colisiones, afecta también la velocidad de reacción.
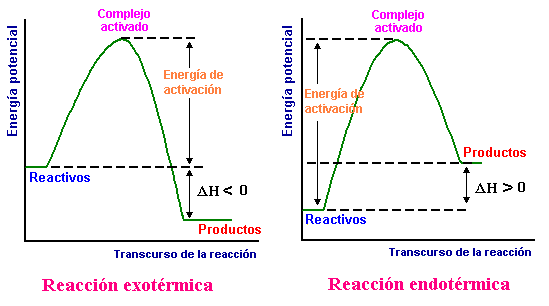
Cuando se produce un choque efectivo, las moléculas involucradas forman una sustancia intermedia, de alta energía, que se denomina complejo activado. La energía de activación Ea, corresponde a la diferencia entre la energía de los reaccionantes y la del complejo activado (figura 4).
Consideremos como ejemplo la formación de agua a partir de hidrógeno y oxígeno gaseosos:
2H2(g) O2(g) 2H2O(g)
Para que se forme el producto, se requiere, en primer lugar que se rompan los enlaces H—H y O—O, para que luego se formen los enlaces H—O. Para que esto suceda, el nivel de energía de las moléculas de H2 y O2 debe ser igual o superior a la Ea y además debe cumplirse que la orientación de la colisión sea la adecuada. En el esquema se puede apreciar que esta reacción libera energía; por lo tanto, se clasifica como exotérmica.
Como se mencionó antes, una reacción química implica una reorganización espacial de los átomos en la ruptura, y posterior formación de enlaces químicos. Para que esto suceda, las moléculas y átomos involucrados, deben estar en contacto físico. Las particularidades del proceso de interacción entre sustancias químicas a nivel molecular se explican a partir de la teoría de las colisiones.
La teoría cinético-molecular de la materia nos dice que los átomos y moléculas de las distintas sustancias se hallan en continuo movimiento, lo que ocasiona choques constantes entre las partículas.
Estos choques son la chispa necesaria para que haya una reacción química. Así, mientras mayor sea el número de choques por unidad de tiempo, mayor será la probabilidad de que ocurra una reacción.
Sin embargo, no todos los choques son efectivos, en el sentido de que provoquen un cambio químico. Para que esto ocurra, las partículas en cuestión deben tener una energía suficientemente alta para vencer las fuerzas de repulsión que actúan entre ellas. De no ser así, dichas partículas se volverían a separar. Por otra parte, debido a que las moléculas suelen tener una compleja estructura tridimensional, alrededor de la cual se distribuyen nubes de electrones, los choques efectivos deben darse en una cierta orientación espacial. En otras palabras, la posición y la dirección con la cual se acerquen las moléculas determinará que se produzca o no una reacción (figura 3).
La energía necesaria para que sea posible una reacción se denomina energía de activación (Ea). La energía de activación es una propiedad de cada reacción y depende de la clase de enlaces que se tengan que romper durante la misma.
De lo anterior se concluye que la velocidad de reacción depende del número de choques por segundo, del número de choques efectivos, de la orientación con la cual ocurren los choques, de la energía que posean las moléculas en el momento de la colisión y de cuánta energía hace falta para alcanzar el valor crítico o energía de activación.
De ahí que, cualquier circunstancia que afecte la frecuencia y la efectividad de las colisiones, afecta también la velocidad de reacción.
Cuando se produce un choque efectivo, las moléculas involucradas forman una sustancia intermedia, de alta energía, que se denomina complejo activado. La energía de activación Ea, corresponde a la diferencia entre la energía de los reaccionantes y la del complejo activado (figura 4).
Consideremos como ejemplo la formación de agua a partir de hidrógeno y oxígeno gaseosos:
2H2(g) O2(g) 2H2O(g)
Para que se forme el producto, se requiere, en primer lugar que se rompan los enlaces H—H y O—O, para que luego se formen los enlaces H—O. Para que esto suceda, el nivel de energía de las moléculas de H2 y O2 debe ser igual o superior a la Ea y además debe cumplirse que la orientación de la colisión sea la adecuada. En el esquema se puede apreciar que esta reacción libera energía; por lo tanto, se clasifica como exotérmica.
FIGURA 3 Partículas de reactivos, con la suficiente energía y orientadas correctamente, chocan de manera efectiva, dando lugar a los productos.
FIGURA 4 Energía de activación y formación del complejo activado, para una reacción endotérmica (a) y exotérmica (b).
EL COMPLEJO ACTIVADO Y LOS PROCESOS ENDOTÉRMICOS Y EXOTÉRMICOS
Existen dos visiones generales acerca de cómo transcurren las reacciones químicas: la teoría de las colisiones y la del complejo activado. La teoría de las colisiones establece que las reacciones proceden, mediante choques efectivos entre las partículas de los reactivos, átomos o moléculas generalmente.
Para que se produzca un choque efectivo se requieren dos condiciones:
1. Que las partículas choquen con una energía mínima suficiente para reorganizar los electrones de valencia, romper unos enlaces y formar otros.
2. Que al chocar, las partículas estén orientadas adecuadamente.
La teoría del complejo activado o del estado de transición describe el curso de una reacción a partir de la variación de energía potencial en los reactivos.
En el punto máximo de la energía entre los reactivos y los productos, se forma una especie química de poca duración y alta energía, que se llama complejo activado.
La diferencia de energía entre el estado inicial de los reactivos y el complejo activado se llama energía de activación y se anota como Ea. Así, los reactivos deben absorber energía suficiente para sobrepasar la energía de activación; de lo contrario, no hay reacción.
La energía de los reactivos, estado inicial es menor que la energía de los productos, estado final.
Desde el complejo activado hasta los productos, se libera una cantidad de energía Ef
La diferencia entre la energía de activación y la energía de formación, es la entalpia E o cambio de calor asociado en la reacción.
E = Ea - Ef
Puesto que se libera más energía desde el complejo activado hasta los productos que la absorbida por los productos hasta el punto máximo, la entalpia de la expresión anterior es negativa, durante la reacción se libera calor, y el proceso es exotérmico.
E = Ea – Ef = -
Considerando la reacción opuesta, es decir, analiznado la reacción desde productos a reactivos, se observa que la energía de los productos, es mayor que la energía de los reactivos; la energía de activación es mayor que de izquierda a derecha.
Desde el complejo activado hasta los productos, se libera energía final o de formación, menor que la liberada de izquierda a derecha, por lo tanto al entalpia es positiva y el proceso es endotérmico. La reacción necesita calor para producirse.
E = Ea – Ef = +
En resumen, una reacción química que es exotérmica de izquierda a derecha, es endotérmica de derecha a izquierda.
Para que se produzca un choque efectivo se requieren dos condiciones:
1. Que las partículas choquen con una energía mínima suficiente para reorganizar los electrones de valencia, romper unos enlaces y formar otros.
2. Que al chocar, las partículas estén orientadas adecuadamente.
La teoría del complejo activado o del estado de transición describe el curso de una reacción a partir de la variación de energía potencial en los reactivos.
En el punto máximo de la energía entre los reactivos y los productos, se forma una especie química de poca duración y alta energía, que se llama complejo activado.
La diferencia de energía entre el estado inicial de los reactivos y el complejo activado se llama energía de activación y se anota como Ea. Así, los reactivos deben absorber energía suficiente para sobrepasar la energía de activación; de lo contrario, no hay reacción.
La energía de los reactivos, estado inicial es menor que la energía de los productos, estado final.
Desde el complejo activado hasta los productos, se libera una cantidad de energía Ef
La diferencia entre la energía de activación y la energía de formación, es la entalpia E o cambio de calor asociado en la reacción.
E = Ea - Ef
Puesto que se libera más energía desde el complejo activado hasta los productos que la absorbida por los productos hasta el punto máximo, la entalpia de la expresión anterior es negativa, durante la reacción se libera calor, y el proceso es exotérmico.
E = Ea – Ef = -
Considerando la reacción opuesta, es decir, analiznado la reacción desde productos a reactivos, se observa que la energía de los productos, es mayor que la energía de los reactivos; la energía de activación es mayor que de izquierda a derecha.
Desde el complejo activado hasta los productos, se libera energía final o de formación, menor que la liberada de izquierda a derecha, por lo tanto al entalpia es positiva y el proceso es endotérmico. La reacción necesita calor para producirse.
E = Ea – Ef = +
En resumen, una reacción química que es exotérmica de izquierda a derecha, es endotérmica de derecha a izquierda.
FACTORES QUE AFECTAN LA VELOCIDAD DE LAS REACCIONES
Teniendo en cuenta los planteamientos de la teoría de las colisiones, cualquier condición que afecte la ocurrencia de choques efectivos, afectará igualmente la velocidad de reacción. Experimentalmente se ha establecido que los principales factores determinantes de la velocidad de las reacciones químicas son: la naturaleza y concentración de los reactivos, la temperatura a la que ocurre la reacción y la presencia de catalizadores.
Naturaleza de los reactivos
La tendencia a reaccionar que muestran unas sustancias con otras se relaciona con la distribución y estructura tridimensional de los electrones periféricos, con la energía de los enlaces que unen los diferentes átomos y con la afinidad entre átomos, moléculas o iones presentes. Por ejemplo, las sustancias en formas moleculares reaccionan más lentamente que las iónicas.
Superficie de contacto
Mientras más puntos de contacto haya entre las sustancias reaccionantes, la reacción ocurrirá más rápido. Por ejemplo, un terrón de azúcar es atacado por bacterias y levaduras, más lentamente que si se hallara disuelto en una solución acuosa
Concentración de los reactivos
A partir de la ecuación de velocidad sabemos que la velocidad es proporcional a la concentración de las especies químicas. Esto se debe a que al aumentar la concentración de las sustancias reaccionantes, se aumenta la probabilidad de choque entre sus moléculas, y por tanto la cantidad de colisiones efectivas. Por ejemplo, un trozo de carbón arde con dificultad si la combustión se realiza en presencia de poco oxígeno, pero si aumentamos la concentración de este gas, la combustión se realiza rápidamente con producción de luz.
Cuando los reactivos son gases, un aumento en la presión del sistema, genera un aumento del número de moléculas por unidad de área, lo que se traduce en un aumento de la concentración que lleva a su vez a una aceleración del proceso.
La magnitud en la cual se aumenta la velocidad, con cada aumento de concentración depende de la reacción y se debe determinar empíricamente.
Temperatura
Con base en la teoría de colisiones, así como en la teoría cinético-molecular, se comprende fácilmente que un aumento en la temperatura del sistema en reacción lleve a un aumento proporcional en la velocidad de reacción. A mayor temperatura, mayor energía cinética poseerán las moléculas y por tanto más cerca estarán de alcanzar el valor crítico, Ea. Así mismo, a mayor energía cinética, la frecuencia de choques se verá también incrementada, y por tanto, la probabilidad de choques efectivos aumentará.
Experimentalmente se ha observado que por cada 10 °C de aumento en la temperatura, la velocidad de reacción se duplica. No obstante, la realidad es un poco más compleja, pues la magnitud del incremento en la velocidad debido a la temperatura depende de la constante específica de la reacción y de la energía de activación.
Naturaleza de los reactivos
La tendencia a reaccionar que muestran unas sustancias con otras se relaciona con la distribución y estructura tridimensional de los electrones periféricos, con la energía de los enlaces que unen los diferentes átomos y con la afinidad entre átomos, moléculas o iones presentes. Por ejemplo, las sustancias en formas moleculares reaccionan más lentamente que las iónicas.
Superficie de contacto
Mientras más puntos de contacto haya entre las sustancias reaccionantes, la reacción ocurrirá más rápido. Por ejemplo, un terrón de azúcar es atacado por bacterias y levaduras, más lentamente que si se hallara disuelto en una solución acuosa
Concentración de los reactivos
A partir de la ecuación de velocidad sabemos que la velocidad es proporcional a la concentración de las especies químicas. Esto se debe a que al aumentar la concentración de las sustancias reaccionantes, se aumenta la probabilidad de choque entre sus moléculas, y por tanto la cantidad de colisiones efectivas. Por ejemplo, un trozo de carbón arde con dificultad si la combustión se realiza en presencia de poco oxígeno, pero si aumentamos la concentración de este gas, la combustión se realiza rápidamente con producción de luz.
Cuando los reactivos son gases, un aumento en la presión del sistema, genera un aumento del número de moléculas por unidad de área, lo que se traduce en un aumento de la concentración que lleva a su vez a una aceleración del proceso.
La magnitud en la cual se aumenta la velocidad, con cada aumento de concentración depende de la reacción y se debe determinar empíricamente.
Temperatura
Con base en la teoría de colisiones, así como en la teoría cinético-molecular, se comprende fácilmente que un aumento en la temperatura del sistema en reacción lleve a un aumento proporcional en la velocidad de reacción. A mayor temperatura, mayor energía cinética poseerán las moléculas y por tanto más cerca estarán de alcanzar el valor crítico, Ea. Así mismo, a mayor energía cinética, la frecuencia de choques se verá también incrementada, y por tanto, la probabilidad de choques efectivos aumentará.
Experimentalmente se ha observado que por cada 10 °C de aumento en la temperatura, la velocidad de reacción se duplica. No obstante, la realidad es un poco más compleja, pues la magnitud del incremento en la velocidad debido a la temperatura depende de la constante específica de la reacción y de la energía de activación.
CONCEPTO DE EQUILIBRIO QUIMICO
El comportamiento general de toda reacción reversible, que en general se puede expresar como:
A2 + B2 2AB
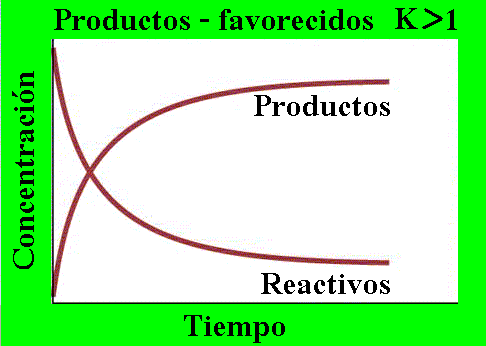
A medida que pasa el tiempo, la velocidad de la reacción hacia la derecha decrece, pero nunca llega a cero. El proceso no se detiene, y la velocidad de la reacción hacia la izquierda aumenta. El equilibrio se establece cuando la velocidad de la reacción hacia la derecha es igual a la de la reacción hacia la izquierda. Por tanto, las concentraciones de todas las especies permanecen constantes.
EN EL EQUILIBRIO EL PROCESO NO SE DETIENE
Una vez una reacción ha llegado a su estado de equilibrio, no se observan cambios en las concentraciones de reactivos y productos. Se puede llegar a pensar que todo proceso ha cesado completamente, lo cual no es cierto: en las moléculas, existe gran movimiento.
La siguiente analogía puede ayudar a entender el concepto de equilibrio químico como igualdad de velocidades.
En un aula de clase que tiene una sola puerta, hay 30 alumnos, los cuales se dividen en dos grupos, no necesariamente de 15. Por ejemplo, 20 estan fuera del aula y 10 estan dentro. El profesor, situado cerca de la puerta, controla que al mismo tiempo un estudiante entre y otro salga; dos estudiantes entran y dos salgan; tres estudiantes entran y tres salen. Mientras el numero de alumnos que entra sea igual al que salga y lo hagan al mismo tiempo, el numero de estudiantes en el salón y fuera de este será la misma cantidad inicial.
En estas condiciones se dice qu existe un equilibrio químico. El equilibrio químico es un equilibrio dinamico.
LA CONSTANTE DE EQUILIBRIO
Se ha establecido que una reacción reversible es de tipo:
A2 + B2 2AB
Alcanza un estado de equilibrio cuando la velocidad de reacción hacia la derecha Vd es igual a la velocidad hacia la izquierda Vi. Por otra parte, se estableció que, para una reacción dada, experimentalmente se puede determinar una ecuación de velocidad, que incluye una constante K y las concentraciones de los reactivos elevados a ciertos exponentes.
Vd = K1 A2 . B2
VI = K2 AB 2
En equilibrio Vd = Vi
Transponiendo términos se tiene:
K1/K2 = AB2 / A2 . B2
El cociente de estas dos constantes de velocidad K1 y K2 es otra constante K, llamada constante de equilibrio, por tanto:
K = AB2 / A2 . B2
Para una ecuación general del tipo analizado, recuerde que AB2, A2, B2 indican concentraciones en moles/litro. Para cada reacción, existe un valor de esta constante que varia con la temperatura. Sin embargo, para una temperatura determinada, ese valor siempre es el mismo, ya que, una vez establecido en equilibrio, las concentraciones de los reactivos y de los productos se mantienen constantes.
Cuando en una reacción química en equilibrio existen varios reactivos y varios productos, a partir de la ecuación estequiomètrica se puede escribir la expresión matemática de K, como se ilustra a continuación:
Aa + Bb + Cc Dd + Ee
K = Dd . Ee / Aa + Bb + Cc minusculas son exponentes
En las ecuaciones de velocidad, los exponentes se determinan experimentalmente. En las constantes de equilibrio, estos exponentes son los coeficientes de la respectiva ecuación estequiomètrica.
A diferencia de las ecuaciones de velocidad, los exponentes en las concentraciones presentes en las constantes de equilibrio son los coeficientes de las ecuaciones balanceadas.
Por convención, las concentraciones de las especies químicas que aparecen en el numerador corresponden a las del lado derecho de la ecuación, esto es, a las concentraciones de los productos.
Esto quiere decir que las reacciones se leen de izquierda a derecha.
La Ki es el inverso de la constante de equilibrio, para la ecuación anterior seria:
Ki = Aa + Bb + Cc / Dd . Ee
Ki = 1 / K
EJEMPLOS
· Para la siguiente ecuación, escriba una expresión de su constante de equilibrio:
NO2 N2O4
Se da una ecuación química sin balancear y se pide una expresión de K. antes de escribir la expresión, debe balancearse la ecuación.
2 NO2 N2O4
K = N2O4 / (NO2)2
· Para cada uno de los siguientes casos, escriba la expresión de K:
o H2 + I2 HI
o NO2 + CO NO + CO2
o H2 + N2 2NH3
o CO2 + H2 CO + H2O
A2 + B2 2AB
A medida que pasa el tiempo, la velocidad de la reacción hacia la derecha decrece, pero nunca llega a cero. El proceso no se detiene, y la velocidad de la reacción hacia la izquierda aumenta. El equilibrio se establece cuando la velocidad de la reacción hacia la derecha es igual a la de la reacción hacia la izquierda. Por tanto, las concentraciones de todas las especies permanecen constantes.
EN EL EQUILIBRIO EL PROCESO NO SE DETIENE
Una vez una reacción ha llegado a su estado de equilibrio, no se observan cambios en las concentraciones de reactivos y productos. Se puede llegar a pensar que todo proceso ha cesado completamente, lo cual no es cierto: en las moléculas, existe gran movimiento.
La siguiente analogía puede ayudar a entender el concepto de equilibrio químico como igualdad de velocidades.
En un aula de clase que tiene una sola puerta, hay 30 alumnos, los cuales se dividen en dos grupos, no necesariamente de 15. Por ejemplo, 20 estan fuera del aula y 10 estan dentro. El profesor, situado cerca de la puerta, controla que al mismo tiempo un estudiante entre y otro salga; dos estudiantes entran y dos salgan; tres estudiantes entran y tres salen. Mientras el numero de alumnos que entra sea igual al que salga y lo hagan al mismo tiempo, el numero de estudiantes en el salón y fuera de este será la misma cantidad inicial.
En estas condiciones se dice qu existe un equilibrio químico. El equilibrio químico es un equilibrio dinamico.
LA CONSTANTE DE EQUILIBRIO
Se ha establecido que una reacción reversible es de tipo:
A2 + B2 2AB
Alcanza un estado de equilibrio cuando la velocidad de reacción hacia la derecha Vd es igual a la velocidad hacia la izquierda Vi. Por otra parte, se estableció que, para una reacción dada, experimentalmente se puede determinar una ecuación de velocidad, que incluye una constante K y las concentraciones de los reactivos elevados a ciertos exponentes.
Vd = K1 A2 . B2
VI = K2 AB 2
En equilibrio Vd = Vi
Transponiendo términos se tiene:
K1/K2 = AB2 / A2 . B2
El cociente de estas dos constantes de velocidad K1 y K2 es otra constante K, llamada constante de equilibrio, por tanto:
K = AB2 / A2 . B2
Para una ecuación general del tipo analizado, recuerde que AB2, A2, B2 indican concentraciones en moles/litro. Para cada reacción, existe un valor de esta constante que varia con la temperatura. Sin embargo, para una temperatura determinada, ese valor siempre es el mismo, ya que, una vez establecido en equilibrio, las concentraciones de los reactivos y de los productos se mantienen constantes.
Cuando en una reacción química en equilibrio existen varios reactivos y varios productos, a partir de la ecuación estequiomètrica se puede escribir la expresión matemática de K, como se ilustra a continuación:
Aa + Bb + Cc Dd + Ee
K = Dd . Ee / Aa + Bb + Cc minusculas son exponentes
En las ecuaciones de velocidad, los exponentes se determinan experimentalmente. En las constantes de equilibrio, estos exponentes son los coeficientes de la respectiva ecuación estequiomètrica.
A diferencia de las ecuaciones de velocidad, los exponentes en las concentraciones presentes en las constantes de equilibrio son los coeficientes de las ecuaciones balanceadas.
Por convención, las concentraciones de las especies químicas que aparecen en el numerador corresponden a las del lado derecho de la ecuación, esto es, a las concentraciones de los productos.
Esto quiere decir que las reacciones se leen de izquierda a derecha.
La Ki es el inverso de la constante de equilibrio, para la ecuación anterior seria:
Ki = Aa + Bb + Cc / Dd . Ee
Ki = 1 / K
EJEMPLOS
· Para la siguiente ecuación, escriba una expresión de su constante de equilibrio:
NO2 N2O4
Se da una ecuación química sin balancear y se pide una expresión de K. antes de escribir la expresión, debe balancearse la ecuación.
2 NO2 N2O4
K = N2O4 / (NO2)2
· Para cada uno de los siguientes casos, escriba la expresión de K:
o H2 + I2 HI
o NO2 + CO NO + CO2
o H2 + N2 2NH3
o CO2 + H2 CO + H2O
| concepto_de_eequilibrio_quimico.docx | |
| File Size: | 3375 kb |
| File Type: | docx |
| cinetica-y-equilibrio.pdf | |
| File Size: | 689 kb |
| File Type: | |