Teoría atómica de Dalton
En 1805 el inglés John Dalton (1766-1844), publicó la obra Nuevo sistema de la fi losofía química, en la cual rescataba las ideas propuestas por Demócrito y Leucipo dos mil años atrás. La razón que impulsó a Dalton a proponer una nueva teoría atómica fue la búsqueda de una explicación a las leyes químicas que se habían deducido empíricamente hasta el momento, como la ley de la conservación y la ley de las proporciones definidas.
La teoría atómica de Dalton comprendía los siguientes postulados:
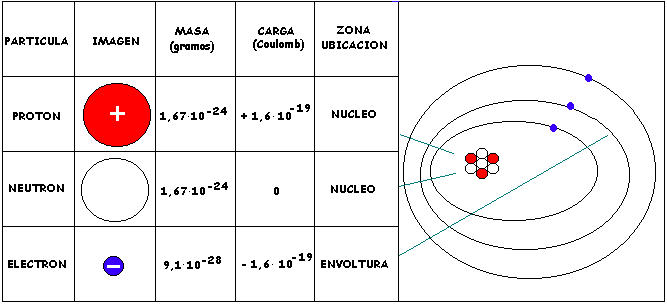
Todo átomo está formado por dos partes, que son:
a) Núcleo atómico: corresponde a la zona central. En él se encuentra la mayor masa del átomo.
b) Corteza atómica: corresponde a la zona que rodea al núcleo. Es la parte más voluminosa del átomo.
Partículas sub-atómicas
¿Existe algo más? Sí. Tanto en el núcleo como en la corteza se ubican varias partículas muy pequeñas; son las llamadas partículas sub-atómicas.
Existen 3 tipos de partículas sub-atómicas.
La teoría atómica de Dalton comprendía los siguientes postulados:
- La materia está constituida por átomos, partículas indivisibles e indestructibles.
- Los átomos que componen una sustancia elemental son semejantes entre sí, en cuanto a masa, tamaño y cualquier otra característica, y difieren de aquellos que componen otros elementos.
- Los átomos se combinan para formar entidades compuestas. En esta combinación los átomos de cada uno de los elementos involucrados están presentes siguiendo proporciones definidas y enteras. Así mismo, dos o más elementos pueden unirse en diferentes proporciones para formar diferentes compuestos.
Todo átomo está formado por dos partes, que son:
a) Núcleo atómico: corresponde a la zona central. En él se encuentra la mayor masa del átomo.
b) Corteza atómica: corresponde a la zona que rodea al núcleo. Es la parte más voluminosa del átomo.
Partículas sub-atómicas
¿Existe algo más? Sí. Tanto en el núcleo como en la corteza se ubican varias partículas muy pequeñas; son las llamadas partículas sub-atómicas.
Existen 3 tipos de partículas sub-atómicas.
Número atómico (Z)
El número atómico indica el número de protones presentes en el núcleo y se representan con la letra Z. Dado que la carga de un átomo es nula, el número de protones debe ser igual al número de electrones, por lo que Z también indica cuántos electrones posee un átomo. Por ejemplo, el átomo de hidrógeno, el más sencillo que se conoce, tiene un núcleo compuesto por un protón que es neutralizado por un electrón orbitando alrededor. De esta manera su número atómico es Z _ 1. Debido a que el número atómico se puede determinar experimentalmente, es posible determinar si una sustancia dada es o no un elemento puro, pues en un elemento todos los átomos deben tener el mismo número atómico.
Número de masa (A)
El número de masa o número másico se representa con la letra A y hace referencia al número de protones y neutrones presentes en el núcleo.
La masa del átomo está concentrada en el núcleo y corresponde a la suma de la masa de los protones y los neutrones presentes, dado que la masa de los electrones es despreciable en relación con la masa nuclear, el número másico también es un indicador indirecto de la masa atómica. Consideremos el siguiente ejemplo: el elemento sodio contiene 11 protones y 12 neutrones en su núcleo. Esto significa que Z es igual a 11 y A es igual a 23, es decir, la suma de 11 protones y 12 neutrones. El número de neutrones presente suele representarse con la letra N.
Z: 11; N: 12 A: N+Z, es decir, A: 12 +11: 23
La masa del átomo está concentrada en el núcleo y corresponde a la suma de la masa de los protones y los neutrones presentes, dado que la masa de los electrones es despreciable en relación con la masa nuclear, el número másico también es un indicador indirecto de la masa atómica. Consideremos el siguiente ejemplo: el elemento sodio contiene 11 protones y 12 neutrones en su núcleo. Esto significa que Z es igual a 11 y A es igual a 23, es decir, la suma de 11 protones y 12 neutrones. El número de neutrones presente suele representarse con la letra N.
Z: 11; N: 12 A: N+Z, es decir, A: 12 +11: 23
Isótopos
Son átomos de un mismo elemento, cuyos núcleos tienen el mismo número de protones (número atómico Z), pero difieren en el número de neutrones (número de masa A). Muchos elementos presentan isótopos, por ejemplo el oxígeno en estado natural es una mezcla de isótopos, en la cual, el 99,8% corresponde a átomos con A _ 16 (Z : 8 y N : 8), el 0,037% poseen A :17
(Z : 8 y N : 9) y el 0,204% está representado por átomos con A : 18 (Z : 8 y N : 10). Esta situación se representa escribiendo el símbolo del elemento y colocando al lado izquierdo, el número de masa (A) del isótopo como un supraíndice y el número atómico (Z) como un subíndice. Veamos algunos ejemplos:
■ Átomo de oxígeno (16, 17 y 18) 16O8 17O8 18O8
(Z : 8 y N : 9) y el 0,204% está representado por átomos con A : 18 (Z : 8 y N : 10). Esta situación se representa escribiendo el símbolo del elemento y colocando al lado izquierdo, el número de masa (A) del isótopo como un supraíndice y el número atómico (Z) como un subíndice. Veamos algunos ejemplos:
■ Átomo de oxígeno (16, 17 y 18) 16O8 17O8 18O8
MASA ATOMICA
La masa atómica relativa de un elemento, es la masa en gramos de 6.02 ·1023 átomos (número de Avogadro, NA) de ese elemento, la masa relativa de los elementos de la tabla periódica desde el 1 hasta el 105 está situada en la parte inferior de los símbolos de dichos elementos. El átomo de carbono, con 6 protones y 6 neutrones, es el átomo de carbono 12 y es la masa de referencia para las masas atómicas. Una unidad de masa atómica (u.m.a), se define exactamente como 1/12 de la masa de un átomo de carbono que tiene una masa 12 u.m.a. una masa atómica relativa molar de carbono 12 tiene una masa de 12 g en esta escala. Un mol gramo (abreviado, mol) de un elemento se define como el numero en gramos de ese elemento igual al número que expresa su masa relativa molar. Así, por ejemplo, un mol gramo de aluminio tiene una masa de 26.98 g y contiene 6.023 ·1023 átomos.
Masa molecular
La masa molecular corresponde a la masa de una molécula, que es igual a la suma de las masas atómicas promedio de los átomos que la constituyen.
Para calcular la masa molecular es necesario saber qué elementos forman el compuesto, su masa atómica y el número de átomos presentes en la molécula.
La fórmula química nos indica qué elementos forman el compuesto y su número.
Para calcular la masa molecular es necesario saber qué elementos forman el compuesto, su masa atómica y el número de átomos presentes en la molécula.
La fórmula química nos indica qué elementos forman el compuesto y su número.
Número de Avogadro: concepto de mol
Cuando tomamos una pequeña cantidad de algún compuesto y la pesamos en una balanza corriente, estamos manipulando un número enorme de átomos individuales, debido a que el peso en gramos de un átomo es sumamente pequeño. Para evitar el problema de hacer cálculos a partir de números muy grandes o muy pequeños, se emplea una unidad, llamada mol.
Un mol se define como la cantidad de sustancia que contiene 6,023X1023 partículas, ya sea de un elemento o de un compuesto. En un elemento esta cantidad es equivalente a la masa atómica expresada como gramos. Por ejemplo, en 15,99 gramos de oxígeno hay exactamente 6,02x1023 átomos de oxígeno. A este número se le conoce como número de Avogadro, pues fue el químico italiano Amadeo Avogadro (1776- 1856) quien estableció esta regla. Avogadro descubrió que volúmenes iguales de diferentes gases, bajo las mismas condiciones de temperatura y presión, contenían igual número de moléculas.
Si una misma cantidad de átomos de dos elementos diferentes, tiene masas diferentes, podemos establecer qué tan pesado es uno con relación al otro. Así, si un mol de oxígeno pesa 16 g, mientras que un mol de carbono pesa 12 g, podemos concluir fácilmente que los átomos de oxígeno son más pesados que los de carbono.
El número de Avogadro es un concepto muy importante y de gran utilidad en química. Por ejemplo, sirve para calcular la masa relativa de un átomo de cualquier elemento y el número de átomos o partículas presentes en una masa determinada de una sustancia dada.
1 mol contiene 6,023x1023 partículas, átomos o moléculas cuya masa es igual a la masa del elemento o del compuesto.
Un mol se define como la cantidad de sustancia que contiene 6,023X1023 partículas, ya sea de un elemento o de un compuesto. En un elemento esta cantidad es equivalente a la masa atómica expresada como gramos. Por ejemplo, en 15,99 gramos de oxígeno hay exactamente 6,02x1023 átomos de oxígeno. A este número se le conoce como número de Avogadro, pues fue el químico italiano Amadeo Avogadro (1776- 1856) quien estableció esta regla. Avogadro descubrió que volúmenes iguales de diferentes gases, bajo las mismas condiciones de temperatura y presión, contenían igual número de moléculas.
Si una misma cantidad de átomos de dos elementos diferentes, tiene masas diferentes, podemos establecer qué tan pesado es uno con relación al otro. Así, si un mol de oxígeno pesa 16 g, mientras que un mol de carbono pesa 12 g, podemos concluir fácilmente que los átomos de oxígeno son más pesados que los de carbono.
El número de Avogadro es un concepto muy importante y de gran utilidad en química. Por ejemplo, sirve para calcular la masa relativa de un átomo de cualquier elemento y el número de átomos o partículas presentes en una masa determinada de una sustancia dada.
1 mol contiene 6,023x1023 partículas, átomos o moléculas cuya masa es igual a la masa del elemento o del compuesto.
COMPOSICIÓN CENTESIMAL Y FORMULAS QUÍMICAS
El análisis cualitativo de una sustancia compuesta permite establecer cuáles son los elementos que la forman; el análisis cuantitativo permite establecer el porcentaje de cada uno de ellos.
A partir de la composición centesimal establecida, se procede a determinar la formula empírica y la formula verdadera del compuesto.
Ejemplo: experimentalmente se encontró que un compuesto tiene 48% de Zn y 52% de Cl. Cuál es la fórmula empírica.
Primero se hallan los moles de cada elemento.
Cl: 52 gr x 1 mol / 35 gr: 1,467 moles
Zn: 48 gr x 1 mol / 65 gr: 0,734 moles
Segundo se busca la relación de números enteros, para obtenerla se divide cada numero de esta relación por el número menor.
Cl: 1,467 / 0,734: 2
Zn: 0,734 / 0,734: 1
Por lo tanto la formula empírica del compuesto es ZnCl2
Con frecuencia para cálculos químicos se requiere conocer el porcentaje en peso de cada uno de los elementos de un compuesto, este porcentaje se puede obtener multiplicando la fracción total de peso de un elemento por 100.
La composición centesimal indica el porcentaje en masa, de cada elemento que forma parte de un compuesto. Se obtiene por análisis gravimétrico y conociendo los pesos atómicos de los compuestos puede determinarse su fórmula mínima o molecular.
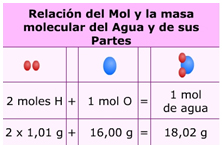
1) La fórmula del agua es H2O. Hallar la composición centesimal del agua
En una molécula de agua hay 2 átomos de hidrógeno y 1 átomo de oxígeno. Su peso molecular corresponde a:
PM del agua = 2 x Pat del H + 1 x Pat del O
PM del H2O = (2 x 1,008) + (1 x 16,000)
Gramos totales = PM del H2O = 18,016 g
En este peso molecular corresponden 2 x 1,008 = 2,016 g de hidrógeno y 16,000 g de oxígeno. Por consiguiente la proporción de estos dos elementos en el agua será:
% elemento = (gramos del elemento / gramos totales) x 100
% H = (2 x 1,008 g / 18,016 g) x 100 =
%H = 0, 1119 x 100 = 11.19 % de Hidrógeno
%O = (16 g / 18,016 g) x 100 =
%O = 0.8881 x 100 = 88.81 % de Oxígeno
Por consiguiente, el agua está constituida por:
elemento---------- % del elemento
Hidrógeno---------- 11,19 % de H
Oxígeno------------ 88.81% de O
Siguiendo el procedimiento anterior, resuelve los siguientes problemas:
2) Hallar la composición centesimal del clorato potásico KClO3
Resultado:
elemento --------------% del elemento
K ----------------------31,91 % de K
Cl --------------------- 28,93 % de Cl
O --------------------- 39,16 % de O
3) Calcular el % Cu (tanto por ciento de cobre) existente en los compuestos siguientes:
a) óxido cuproso, Cu2O
b) cloruro cuproso, CuCl
c) sulfuro cúprico, CuS
d) sulfato cúprico pentahidratado CuCO4.H2O
Resultado:
ejercicio ----------------% Cu
a) ----------------------88,85 % de Cu
b) ----------------------64,20 % de Cu
c) ----------------------66,46 % de Cu
d) ----------------------25,45 % de Cu
Calcular la composición centesimal del H2O
pesos atómicos: H = 1 , O = 16
A partir de la composición centesimal establecida, se procede a determinar la formula empírica y la formula verdadera del compuesto.
Ejemplo: experimentalmente se encontró que un compuesto tiene 48% de Zn y 52% de Cl. Cuál es la fórmula empírica.
Primero se hallan los moles de cada elemento.
Cl: 52 gr x 1 mol / 35 gr: 1,467 moles
Zn: 48 gr x 1 mol / 65 gr: 0,734 moles
Segundo se busca la relación de números enteros, para obtenerla se divide cada numero de esta relación por el número menor.
Cl: 1,467 / 0,734: 2
Zn: 0,734 / 0,734: 1
Por lo tanto la formula empírica del compuesto es ZnCl2
- La composición centesimal de un compuesto:
Con frecuencia para cálculos químicos se requiere conocer el porcentaje en peso de cada uno de los elementos de un compuesto, este porcentaje se puede obtener multiplicando la fracción total de peso de un elemento por 100.
La composición centesimal indica el porcentaje en masa, de cada elemento que forma parte de un compuesto. Se obtiene por análisis gravimétrico y conociendo los pesos atómicos de los compuestos puede determinarse su fórmula mínima o molecular.
1) La fórmula del agua es H2O. Hallar la composición centesimal del agua
En una molécula de agua hay 2 átomos de hidrógeno y 1 átomo de oxígeno. Su peso molecular corresponde a:
PM del agua = 2 x Pat del H + 1 x Pat del O
PM del H2O = (2 x 1,008) + (1 x 16,000)
Gramos totales = PM del H2O = 18,016 g
En este peso molecular corresponden 2 x 1,008 = 2,016 g de hidrógeno y 16,000 g de oxígeno. Por consiguiente la proporción de estos dos elementos en el agua será:
% elemento = (gramos del elemento / gramos totales) x 100
% H = (2 x 1,008 g / 18,016 g) x 100 =
%H = 0, 1119 x 100 = 11.19 % de Hidrógeno
%O = (16 g / 18,016 g) x 100 =
%O = 0.8881 x 100 = 88.81 % de Oxígeno
Por consiguiente, el agua está constituida por:
elemento---------- % del elemento
Hidrógeno---------- 11,19 % de H
Oxígeno------------ 88.81% de O
Siguiendo el procedimiento anterior, resuelve los siguientes problemas:
2) Hallar la composición centesimal del clorato potásico KClO3
Resultado:
elemento --------------% del elemento
K ----------------------31,91 % de K
Cl --------------------- 28,93 % de Cl
O --------------------- 39,16 % de O
3) Calcular el % Cu (tanto por ciento de cobre) existente en los compuestos siguientes:
a) óxido cuproso, Cu2O
b) cloruro cuproso, CuCl
c) sulfuro cúprico, CuS
d) sulfato cúprico pentahidratado CuCO4.H2O
Resultado:
ejercicio ----------------% Cu
a) ----------------------88,85 % de Cu
b) ----------------------64,20 % de Cu
c) ----------------------66,46 % de Cu
d) ----------------------25,45 % de Cu
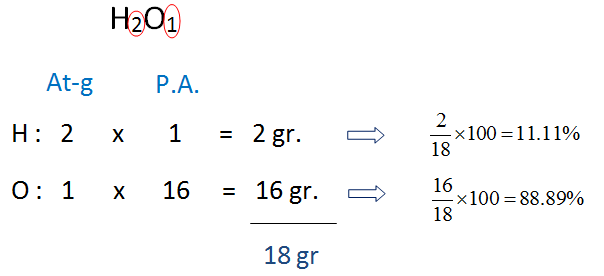
Calcular la composición centesimal del H2O
pesos atómicos: H = 1 , O = 16
Entonces la composición centesimal del agua (H2O) es:
· H = 11.11%
· O = 88.89%
· H = 11.11%
· O = 88.89%
- Formulas y clases de fórmulas:
Existen varias clases de fórmulas químicas:
Empírica o simplificadas.
Molecular y verdadera.
Estructural.
1. Formula empírica o simplificada:
Es aquella en la cual se indica la relación más pequeña en términos de números enteros en que se encuentran los átomos de los elementos que forman el compuesto. Esta formula se deriva directamente de la experimentación, requiere conocer la composición centesimal.
2. Formula molecular o verdadera:
Es aquella que indica el número real de átomos de cada elemento en una molécula. En muchos casos la formula empírica de un compuesto no coincide con la formula verdadera.
Formula molecular formula empírica
C4H10 C2H5
C6H12O6 C1H2O1
CO2 CO2
3. Formula estructural:
En una formula estructural se presenta la distribución y la orientación de los atomos en el espacio, frecuentemente indica los ángulos que se forman entre ellos.
CALCULO DE LA FORMULA EMPIRICA Y MOLECULAR
Para llegar a la formula molecular de una sustancia, es preciso calcular experimentalmente las cantidades de los elementos que reaccionan entre si para formar una cantidad dada de determinado compuesto, usualmente 100 gramos. Esto es calcular su composición centesimal, con el fin de determinar su fórmula empírica.
Calculada la formula empírica, se requiere determinar el peso molecular, para ver si la formula empírica y la formula verdadera son iguales o si la formula verdadera es un múltiplo entero de la empírica.
N= pm/ fe
N: numero entero por el cual se simplifica la formula verdadera.
Pm: peso molecular.
Fe: formula empírica
Ejemplo: el análisis de un hidrocarburo dio la siguiente composición centesimal
C:92,26%, H: 7,74%, si el peso molecular del hidrocarburo es 78 gr ¿Cuál es la fórmula empírica y verdadera del compuesto?
C: 92,26/12= 7,68 moles
H: 7,74/1 = 7,74 moles
C: 7,68/7,74 = 1
H: 7,74/7,74 = 1
Formula empírica C1H1
C: 1 x 12 = 12
H: 1 x 1 = 1
CH = 13
N= 78 gr / 13 = 6
Formula verdadera= (CH)6 = C6H6