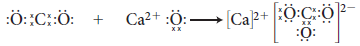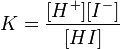EQUILIBRIO EN SOLUCIONES IONICAS
En el siglo XVIII ya se sabía que ciertas soluciones tenían la propiedad de conducir la electricidad, por lo que más tarde se las llamó soluciones de electrólitos.
A continuación, vamos a considerar algunos de las propiedades de estas soluciones, deteniéndonos en dos grupos muy especiales: las soluciones ácidas y las soluciones básicas.
A continuación, vamos a considerar algunos de las propiedades de estas soluciones, deteniéndonos en dos grupos muy especiales: las soluciones ácidas y las soluciones básicas.
| equilibrio_acido_base.pdf | |
| File Size: | 1328 kb |
| File Type: | |
Electrólitos
Un electrólito es una sustancia que se ioniza, es decir, que se disocia, dando lugar a los iones correspondientes. El resultado es una solución conductora de la corriente eléctrica. Ejemplos de solución de electrólitos son las soluciones acuosas de sales, ácidos o bases.
Cuando un soluto no se disocia en iones, sino que por el contrario conserva su naturaleza molecular, se forma una solución que no conduce la corriente eléctrica.
Este tipo de soluciones se conocen como soluciones moleculares o de no electrólitos.
La mayoría de las sustancias orgánicas, como hidrocarburos y azúcares, forman soluciones de no electrólitos.
Los electrólitos se dividen teniendo en cuenta un criterio cualitativo en electrólitos fuertes y electrólitos débiles. Los electrólitos fuertes son compuestos que se disocian prácticamente en su totalidad, dando lugar a soluciones que conducen bien la corriente eléctrica. Por el contrario, los electrólitos débiles son sustancias que se ionizan solo en pequeñas proporciones, con lo cual parte de las moléculas originales no se disocian y por tanto no contribuyen a la conducción de corrientes eléctricas, dando origen a soluciones que no conducen adecuadamente la electricidad.
Hay tres clases de electrólitos fuertes:
Los ácidos fuertes: son ácidos que forman soluciones acuosas diluidas, en las cuales cerca del 100% de las moléculas se ionizan. Los más comunes son el ácido sulfúrico (H2SO4), el ácido clorhídrico (HCl), el ácido nítrico (HNO3), el ácido bromhídrico (HBr), el ácido perclórico (HClO4) y el ácido yodhídrico (HI).
Los ácidos fuertes existen casi exclusivamente como iones en soluciones acuosas diluidas, como en el siguiente ejemplo:
H2SO4(ac) 2H (ac) + SO4(ac)
ac: medio o solución acuosa
Las bases fuertes: se forman generalmente con los metales del grupo IA y algunos del grupo IIA, siendo las más comunes hidróxidos metálicos solubles.
Al igual que los ácidos fuertes, las bases fuertes se caracterizan porque se ionizan casi completamente en soluciones acuosas diluidas, como se muestra a continuación para el hidróxido de sodio (NaOH) en solución acuosa:
NaOH(ac) Na(ac) + OH(ac)
Las sales solubles: la mayor parte de las sales solubles son compuestos iónicos, tanto en estado sólido como en solución. Por ejemplo, el proceso de disociación para el cloruro de sodio se puede representar así:
NaCl(ac) Na (ac) + Cl (ac)
Cuando un soluto no se disocia en iones, sino que por el contrario conserva su naturaleza molecular, se forma una solución que no conduce la corriente eléctrica.
Este tipo de soluciones se conocen como soluciones moleculares o de no electrólitos.
La mayoría de las sustancias orgánicas, como hidrocarburos y azúcares, forman soluciones de no electrólitos.
Los electrólitos se dividen teniendo en cuenta un criterio cualitativo en electrólitos fuertes y electrólitos débiles. Los electrólitos fuertes son compuestos que se disocian prácticamente en su totalidad, dando lugar a soluciones que conducen bien la corriente eléctrica. Por el contrario, los electrólitos débiles son sustancias que se ionizan solo en pequeñas proporciones, con lo cual parte de las moléculas originales no se disocian y por tanto no contribuyen a la conducción de corrientes eléctricas, dando origen a soluciones que no conducen adecuadamente la electricidad.
Hay tres clases de electrólitos fuertes:
Los ácidos fuertes: son ácidos que forman soluciones acuosas diluidas, en las cuales cerca del 100% de las moléculas se ionizan. Los más comunes son el ácido sulfúrico (H2SO4), el ácido clorhídrico (HCl), el ácido nítrico (HNO3), el ácido bromhídrico (HBr), el ácido perclórico (HClO4) y el ácido yodhídrico (HI).
Los ácidos fuertes existen casi exclusivamente como iones en soluciones acuosas diluidas, como en el siguiente ejemplo:
H2SO4(ac) 2H (ac) + SO4(ac)
ac: medio o solución acuosa
Las bases fuertes: se forman generalmente con los metales del grupo IA y algunos del grupo IIA, siendo las más comunes hidróxidos metálicos solubles.
Al igual que los ácidos fuertes, las bases fuertes se caracterizan porque se ionizan casi completamente en soluciones acuosas diluidas, como se muestra a continuación para el hidróxido de sodio (NaOH) en solución acuosa:
NaOH(ac) Na(ac) + OH(ac)
Las sales solubles: la mayor parte de las sales solubles son compuestos iónicos, tanto en estado sólido como en solución. Por ejemplo, el proceso de disociación para el cloruro de sodio se puede representar así:
NaCl(ac) Na (ac) + Cl (ac)
Equilibrios de solubilidad
Como acabamos de mencionar, en soluciones de electrólitos fuertes, la totalidad de las moléculas se encuentran disociadas, es decir, las reacciones que describen el proceso de disolución ocurren principalmente hacia la derecha, como por ejemplo en el siguiente caso:
HCl(ac) H(ac) + Cl(ac)
Se trata de sistemas que no están en equilibrio, pues la velocidad hacia la derecha es varias veces superior a la velocidad hacia la izquierda.
Por el contrario, en una solución de un electrólito débil, parte de las moléculas se halla disociada y parte conserva su estado molecular, situación en la cual se alcanza un estado de equilibrio.
Para el ácido acético podemos representar esta situación como sigue:
CH3COOH(ac) CH3COO(ac) + H(ac)
Veamos a continuación el proceso de disociación de las tres clases principales de electrólitos: ácidos, bases y sales.
Disociación de ácidos. Cuando estas sustancias se disuelven en agua, son atraídas por los polos positivo y negativo de la molécula de agua, con lo cual se produce la disociación de la molécula de ácido. Durante este proceso se liberan iones H1, llamados hidrogeniones. Se trata de átomos de hidrógeno, que al carecer del electrón correspondiente actúan como partículas positivas o protones.
La disociación de un ácido cualquiera se puede representar así:
HA(ac) H(ac) + A(ac)
Si el ácido es un electrólito fuerte, la disociación se produce en un 100% y la probabilidad de la reacción reversible es prácticamente nula. Si el ácido es un electrólito débil, los iones formados tienden a agruparse nuevamente, haciendo que se establezca un equilibrio entre el ácido y los iones. Como en cualquier situación donde se presente un estado de equilibrio, se puede calcular la constante de equilibrio para la solución, denominada constante de disociación, Kd. Cuando se trata de un ácido, se le llama constante de acidez, Ka. Para la reacción anterior:
Ka = H. A
HA
Disociación de bases. Es un proceso similar al descrito para sustancias ácidas, pero donde se liberan iones OH2 o hidróxilo.
Para bases débiles, se establece rápidamente un estado de equilibrio iónico, para el cual se tiene una constante de disociación, conocida como constante de basicidad, Kb (fi gura 3). En forma general el proceso para una base se representa así:
MOH(ac) M(ac) + OH(ac)
Donde Kb será igual a:
Kb = M . OH
MOH
Disociación de sales. La mayoría de las sales son solubles en agua y establecen situaciones de no equilibrio, en las que todas las moléculas se hallan disociadas. En cambio, cuando una sal poco soluble se disuelve en agua, se alcanza un equilibrio entre los procesos de disolución y precipitación, según se representa en la siguiente ecuación:
MA(s) M(ac) + A (ac), donde Kd = A . M
Observa que la expresión para Kd no tiene denominador, pues la especie MA es un sólido. Recordemos que la concentración molecular de los productos sólidos y de los líquidos puros no varía, y por lo tanto el valor de la constante solo depende de las concentraciones de los iones disueltos. Para las sales decimos que la constante de disociación es igual a:
Kd = Ke = Kps,
Donde Kps es la constante del producto de solubilidad.
Grado de disociación. Empleamos el término grado de disociación (a) para cuantificar qué tanto se disocia un soluto, a se obtiene de la relación entre el número de moles disociadas y el número de moles iniciales o totales, según la expresión:
a = No. de moles que se disocian . 100
No. de moles totales
Por ejemplo, si en una solución 1 M de H3PO4, la concentración de H, una vez alcanzado el equilibrio es de 0,10 M, el grado de disociación para la solución es:
a = No. De moles que se disocian . 100
No. De moles totales
a = 0.10 M . 100
1M
A continuación desarrollaremos dos ejemplos de cómo calcular la constante de disociación y las concentraciones iónicas en el equilibrio.
HCl(ac) H(ac) + Cl(ac)
Se trata de sistemas que no están en equilibrio, pues la velocidad hacia la derecha es varias veces superior a la velocidad hacia la izquierda.
Por el contrario, en una solución de un electrólito débil, parte de las moléculas se halla disociada y parte conserva su estado molecular, situación en la cual se alcanza un estado de equilibrio.
Para el ácido acético podemos representar esta situación como sigue:
CH3COOH(ac) CH3COO(ac) + H(ac)
Veamos a continuación el proceso de disociación de las tres clases principales de electrólitos: ácidos, bases y sales.
Disociación de ácidos. Cuando estas sustancias se disuelven en agua, son atraídas por los polos positivo y negativo de la molécula de agua, con lo cual se produce la disociación de la molécula de ácido. Durante este proceso se liberan iones H1, llamados hidrogeniones. Se trata de átomos de hidrógeno, que al carecer del electrón correspondiente actúan como partículas positivas o protones.
La disociación de un ácido cualquiera se puede representar así:
HA(ac) H(ac) + A(ac)
Si el ácido es un electrólito fuerte, la disociación se produce en un 100% y la probabilidad de la reacción reversible es prácticamente nula. Si el ácido es un electrólito débil, los iones formados tienden a agruparse nuevamente, haciendo que se establezca un equilibrio entre el ácido y los iones. Como en cualquier situación donde se presente un estado de equilibrio, se puede calcular la constante de equilibrio para la solución, denominada constante de disociación, Kd. Cuando se trata de un ácido, se le llama constante de acidez, Ka. Para la reacción anterior:
Ka = H. A
HA
Disociación de bases. Es un proceso similar al descrito para sustancias ácidas, pero donde se liberan iones OH2 o hidróxilo.
Para bases débiles, se establece rápidamente un estado de equilibrio iónico, para el cual se tiene una constante de disociación, conocida como constante de basicidad, Kb (fi gura 3). En forma general el proceso para una base se representa así:
MOH(ac) M(ac) + OH(ac)
Donde Kb será igual a:
Kb = M . OH
MOH
Disociación de sales. La mayoría de las sales son solubles en agua y establecen situaciones de no equilibrio, en las que todas las moléculas se hallan disociadas. En cambio, cuando una sal poco soluble se disuelve en agua, se alcanza un equilibrio entre los procesos de disolución y precipitación, según se representa en la siguiente ecuación:
MA(s) M(ac) + A (ac), donde Kd = A . M
Observa que la expresión para Kd no tiene denominador, pues la especie MA es un sólido. Recordemos que la concentración molecular de los productos sólidos y de los líquidos puros no varía, y por lo tanto el valor de la constante solo depende de las concentraciones de los iones disueltos. Para las sales decimos que la constante de disociación es igual a:
Kd = Ke = Kps,
Donde Kps es la constante del producto de solubilidad.
Grado de disociación. Empleamos el término grado de disociación (a) para cuantificar qué tanto se disocia un soluto, a se obtiene de la relación entre el número de moles disociadas y el número de moles iniciales o totales, según la expresión:
a = No. de moles que se disocian . 100
No. de moles totales
Por ejemplo, si en una solución 1 M de H3PO4, la concentración de H, una vez alcanzado el equilibrio es de 0,10 M, el grado de disociación para la solución es:
a = No. De moles que se disocian . 100
No. De moles totales
a = 0.10 M . 100
1M
A continuación desarrollaremos dos ejemplos de cómo calcular la constante de disociación y las concentraciones iónicas en el equilibrio.
| equilibrio_en_las_disoluciones_de_cidos_dbiles_y_bases_dbiles.docx | |
| File Size: | 42 kb |
| File Type: | docx |
Conceptos y teorías sobre ácidos y bases
Los ácidos y las bases fueron reconocidos inicialmente por sus propiedades más simples, como el sabor: los ácidos tienen un sabor agrio, mientras que las bases son amargas. Posteriormente, se observó que estas sustancias tenían la capacidad de cambiar el color de ciertos compuestos, como el papel de tornasol y la fenolftaleína, que, por esta razón, se conocen como indicadores. Los ácidos viran el papel tornasol de azul a rojo y la fenolftaleína de rojo a incolora, mientras que las bases viran el papel tornasol de rojo a azul y la fenolftaleína de incolora a rosa.
Como se ha explicado ya, ácidos y bases forman soluciones de electrólitos, capaces de conducir la electricidad. No obstante, muestran propiedades químicas diferentes. Por ejemplo, los ácidos reaccionan con ciertos metales, como magnesio, zinc o hierro, produciendo hidrógeno gaseoso. Las bases por su parte no muestran este comportamiento, al tiempo que son muy buenos detergentes, presentando una textura jabonosa.
Así mismo, los ácidos y bases reaccionan entre sí dando como resultado una solución compuesta por una sal y agua, que si bien conduce la electricidad, no tiene las propiedades físico-químicas que tienen ácidos y bases independientemente.
En un intento por dar una explicación al porqué los ácidos y las bases se comportan física y químicamente como lo hacen, se han propuesto una serie de teorías sobre ellos, llamadas teorías ácido-base. Veamos.
Teoría de Svante Arrhenius
El químico sueco Svante Arrhenius (1859-1927) formuló en 1884 el primer concepto teórico sobre el comportamiento de ácidos y bases, partiendo del efecto que tienen estas sustancias sobre el agua, cuando se encuentran formando soluciones acuosas. Arrhenius propuso que: un ácido es una sustancia que cuando se disuelve en agua incrementa la concentración de iones hidrógeno, H1. Mientras que, una base se define como toda sustancia capaz de incrementar la concentración de iones hidroxilo, OH2, en solución acuosa. La teoría de Arrhenius tenía algunas limitaciones: se restringía a sustancias en solución acuosa y al definir la condición ácida y básica a partir de la presencia de iones H1 y OH2, desconocía una serie de compuestos que, si bien se comportan como ácido o bases, no se componen de estos iones.
Teoría de Brönsted-Lowry
En 1923, en forma simultánea, pero por separado, los químicos Johannes Brönsted (1879-1947) y Thomas Lowry (1874-1936) propusieron que las reacciones ácido-base podían ser interpretadas como transferencias de protones entre los compuestos involucrados. Sobre esta base, aportaron una definición más amplia de ácidos y bases, según la cual, un ácido es una especie capaz de ceder uno o más protones (iones H1), en tanto que una base es una sustancia capaz de aceptar dichos protones.
De esta manera, cuando un ácido dona un protón, da origen a una base conjugada, que es una especie capaz de volver a captar el protón cedido. Igualmente, una base se disocia para dar lugar a un ion OH2, que es capaz de aceptar un protón, con lo que forma un ácido conjugado.
Estos conceptos se resumen en las siguientes reacciones esquemáticas:
Ácido Base conjugada + H
Base + H Ácido conjugado
En este contexto, una reacción de neutralización se puede representar así:
ácido1 + base2 base conjugada1 + ácido conjugado2
Veamos dos ejemplos, el primero para la disociación de un ácido, como el ácido cianhídrico y el segundo para un ácido (HCl) y una base (NH3)
HCN + H2O CN + H3O
HCl + NH3 Cl + NH4
Teoría de Lewis
Bajo los conceptos de ácido y base planteados por el químico norteamericano Gilbert Lewis (1875-1946), en 1938, se alcanzó una mayor generalización, que permitió incluir dentro de la definición compuestos que antes no encajaban. Por ejemplo, la reacción entre el dióxido de carbono y el óxido de calcio constituye una interacción ácido-base, desde la teoría de Lewis, que se basa en la donación de pares de electrones en enlaces covalentes.
CO2 + CaO Ca + CO3
Así, un ácido de Lewis se define como toda sustancia capaz de aceptar pares de electrones, mientras que una base de Lewis es una sustancia que puede ceder pares de electrones.
Esta definición implica que las moléculas de los ácidos deben poseer orbitales vacíos para alojar electrones, al tiempo que las bases deben tener llenos los orbitales correspondiente, para poder ceder la pareja de electrones libres. Esquemáticamente, representamos esta situación así:
En una reacción de neutralización una sustancia con un hueco electrónico, es decir, un ácido de Lewis acepta un par de electrones cedidos por una base de Lewis. Veamos un ejemplo:
BF3 + :NH3 F3B :NH3
Como se ha explicado ya, ácidos y bases forman soluciones de electrólitos, capaces de conducir la electricidad. No obstante, muestran propiedades químicas diferentes. Por ejemplo, los ácidos reaccionan con ciertos metales, como magnesio, zinc o hierro, produciendo hidrógeno gaseoso. Las bases por su parte no muestran este comportamiento, al tiempo que son muy buenos detergentes, presentando una textura jabonosa.
Así mismo, los ácidos y bases reaccionan entre sí dando como resultado una solución compuesta por una sal y agua, que si bien conduce la electricidad, no tiene las propiedades físico-químicas que tienen ácidos y bases independientemente.
En un intento por dar una explicación al porqué los ácidos y las bases se comportan física y químicamente como lo hacen, se han propuesto una serie de teorías sobre ellos, llamadas teorías ácido-base. Veamos.
Teoría de Svante Arrhenius
El químico sueco Svante Arrhenius (1859-1927) formuló en 1884 el primer concepto teórico sobre el comportamiento de ácidos y bases, partiendo del efecto que tienen estas sustancias sobre el agua, cuando se encuentran formando soluciones acuosas. Arrhenius propuso que: un ácido es una sustancia que cuando se disuelve en agua incrementa la concentración de iones hidrógeno, H1. Mientras que, una base se define como toda sustancia capaz de incrementar la concentración de iones hidroxilo, OH2, en solución acuosa. La teoría de Arrhenius tenía algunas limitaciones: se restringía a sustancias en solución acuosa y al definir la condición ácida y básica a partir de la presencia de iones H1 y OH2, desconocía una serie de compuestos que, si bien se comportan como ácido o bases, no se componen de estos iones.
Teoría de Brönsted-Lowry
En 1923, en forma simultánea, pero por separado, los químicos Johannes Brönsted (1879-1947) y Thomas Lowry (1874-1936) propusieron que las reacciones ácido-base podían ser interpretadas como transferencias de protones entre los compuestos involucrados. Sobre esta base, aportaron una definición más amplia de ácidos y bases, según la cual, un ácido es una especie capaz de ceder uno o más protones (iones H1), en tanto que una base es una sustancia capaz de aceptar dichos protones.
De esta manera, cuando un ácido dona un protón, da origen a una base conjugada, que es una especie capaz de volver a captar el protón cedido. Igualmente, una base se disocia para dar lugar a un ion OH2, que es capaz de aceptar un protón, con lo que forma un ácido conjugado.
Estos conceptos se resumen en las siguientes reacciones esquemáticas:
Ácido Base conjugada + H
Base + H Ácido conjugado
En este contexto, una reacción de neutralización se puede representar así:
ácido1 + base2 base conjugada1 + ácido conjugado2
Veamos dos ejemplos, el primero para la disociación de un ácido, como el ácido cianhídrico y el segundo para un ácido (HCl) y una base (NH3)
HCN + H2O CN + H3O
HCl + NH3 Cl + NH4
Teoría de Lewis
Bajo los conceptos de ácido y base planteados por el químico norteamericano Gilbert Lewis (1875-1946), en 1938, se alcanzó una mayor generalización, que permitió incluir dentro de la definición compuestos que antes no encajaban. Por ejemplo, la reacción entre el dióxido de carbono y el óxido de calcio constituye una interacción ácido-base, desde la teoría de Lewis, que se basa en la donación de pares de electrones en enlaces covalentes.
CO2 + CaO Ca + CO3
Así, un ácido de Lewis se define como toda sustancia capaz de aceptar pares de electrones, mientras que una base de Lewis es una sustancia que puede ceder pares de electrones.
Esta definición implica que las moléculas de los ácidos deben poseer orbitales vacíos para alojar electrones, al tiempo que las bases deben tener llenos los orbitales correspondiente, para poder ceder la pareja de electrones libres. Esquemáticamente, representamos esta situación así:
En una reacción de neutralización una sustancia con un hueco electrónico, es decir, un ácido de Lewis acepta un par de electrones cedidos por una base de Lewis. Veamos un ejemplo:
BF3 + :NH3 F3B :NH3
CONSTANTE DE EQUILIBRIO DEL AGUA
| equilibrio_inico_del_agua.pdf | |
| File Size: | 514 kb |
| File Type: | |
HCl + H2O --> H3O+ + Cl-
Donde:
Keq=[H3O+][Cl-]/[HCl]
En el tiempo de equilibrio [HCl] tiende a cero, por ende Keq tiende a infinito
Cuando la disociación es menor al 100%, se habla de un electrolito débil. Los eletrolitos débiles forman equilibrios verdaderos
Ejemplo: HF + H2O <==> H3O+ + F-
Esta reacción no se completa, alcanza cierto equilibrio, con cierta constante, por eso debe llevar dos medias flechas en direcciones opuestas (flecha doble)
Donde: Keq=[H3O+][F-]/[HF]
Como la disociación no es completa, en el tiempo de equilibrio, [HF], [H3O+] y [F-] permanecerán constante, por ende estamos en presencia de un equilibrio químico.
La autoionización del agua es la reacción química en la que dos moléculas de agua reaccionan para producir un ion hidronio (H3O+) y un ion hidróxido (OH−):
2 H2O (l) H3O+ (aq) + OH− (aq)
El agua es un electrolito débil, por lo que conduce la corriente eléctrica en una fracción pequeñísima, debido a que se encuentra poco disociada.
H2O + H2O = H3O+ + OH-
Al ser una reacción reversible, podemos expresarla en función de una constante de equilibrio:
Keq= [H3O+]·[OH-]
Al ser el agua una especie pura, no se le considera en la expresión, por ende, la constante de equilibrio del agua queda expresada en función de la presencia de los dos iones formados.
Mediante procesos electroquímicos, se pudo comprobar que la constante de equilibrio de esta relación tiene un valor de:
[H3O+] = [OH-] = 1·10-7
Kw=1·10-14
que es conocida como Constante de autoionización del agua
Donde:
Keq=[H3O+][Cl-]/[HCl]
En el tiempo de equilibrio [HCl] tiende a cero, por ende Keq tiende a infinito
Cuando la disociación es menor al 100%, se habla de un electrolito débil. Los eletrolitos débiles forman equilibrios verdaderos
Ejemplo: HF + H2O <==> H3O+ + F-
Esta reacción no se completa, alcanza cierto equilibrio, con cierta constante, por eso debe llevar dos medias flechas en direcciones opuestas (flecha doble)
Donde: Keq=[H3O+][F-]/[HF]
Como la disociación no es completa, en el tiempo de equilibrio, [HF], [H3O+] y [F-] permanecerán constante, por ende estamos en presencia de un equilibrio químico.
La autoionización del agua es la reacción química en la que dos moléculas de agua reaccionan para producir un ion hidronio (H3O+) y un ion hidróxido (OH−):
2 H2O (l) H3O+ (aq) + OH− (aq)
El agua es un electrolito débil, por lo que conduce la corriente eléctrica en una fracción pequeñísima, debido a que se encuentra poco disociada.
H2O + H2O = H3O+ + OH-
Al ser una reacción reversible, podemos expresarla en función de una constante de equilibrio:
Keq= [H3O+]·[OH-]
Al ser el agua una especie pura, no se le considera en la expresión, por ende, la constante de equilibrio del agua queda expresada en función de la presencia de los dos iones formados.
Mediante procesos electroquímicos, se pudo comprobar que la constante de equilibrio de esta relación tiene un valor de:
[H3O+] = [OH-] = 1·10-7
Kw=1·10-14
que es conocida como Constante de autoionización del agua
| equilibrio_inico.docx | |
| File Size: | 55 kb |
| File Type: | docx |
EL pH Y pOH
El concepto de pH (Potencial de Hidrógeno) fue definido por primera vez por Soren Poer Lauritz Sorensen (1868-1939) Bioquímico danés, originalmente Sorensen. En el año de 1909.
La escala de pH fue ideada para expresar en forma adecuada diferentes concentraciones del ión (H+) (ión Hidrógeno), en varias soluciones sin necesidad de utilizar números en forma exponencial, debido a que con frecuencia son números muy pequeños y por lo tanto es difícil trabajar con ellos, fue así entonces que se decidió trabajar con números enteros positivos.
El pH de una disolución se define como el logaritmo negativo de la concentración del ión hidrógeno expresado en (mol/litro), la escala de pH se define por la ecuación:
pH = - log [H+]
El logaritmo negativo proporciona un número positivo para el pH, además el termino [H+] corresponde a la parte numérica de la expresión para la concentración del ión hidrógeno. Debido a que el pH solo es una manera de expresar la concentración del ión hidrógeno, las disoluciones ácidas y básicas (25°C), pueden identificarse por sus valores de pH como sigue:
· Disoluciones acidas: [H+] > 1,0 x 10-7M, pH < 7.00
· Disoluciones básicas: [H+] < 1,0 x 10-7M, pH > 7.00
· Disoluciones neutras: [H+] = 1,0 x 10-7M, pH = 7.00
Se observa que el pH aumenta a medida que el [H+] disminuye.
En el caso del H2O pura, tendremos:
La disociación del H2O es: H2O + H2O ↔ H3O+ + OH-
Por tanto [H3O+] = [OH-] = 1 x 10-7 mol/litro
pH = - log [H3O+]
pH = - log [1 x 10-7]
pH = 7
A 25°C, el pH del agua pura y de cualquier solución acuosa que contenga concentraciones iguales de Ión hidronio y de ión hidroxilo es 7.
Ej: Calcúlese el pH de una solución cuya concentración de ión hidronio es 6,0 x 10 –5 M
pH = - log [6,0 x 10 –5]
= - log [6,0 x 10 –5]
= - [log 6,0 + log 10 –5]
pH = -0,78 + 5 = 4,22
Una escala semejante a la escala del pH puede usarse para expresar la concentración del ión hidroxilo de las soluciones.
El pOH se define como el logaritmo negativo de la concentración molar de iones (OH) es decir:
pOH : - log [OH-]
El pH y el pOH se relacionan así:
[H3O+] [OH-]= 10-14; log [H3O+] [OH-]= log 10-14
Luego log [H3O+] + log [OH-]= - 14 (- log [H3O+])+ (- log [OH-]) = 14
y decir: pH + pOH = 14
La escala de pH fue ideada para expresar en forma adecuada diferentes concentraciones del ión (H+) (ión Hidrógeno), en varias soluciones sin necesidad de utilizar números en forma exponencial, debido a que con frecuencia son números muy pequeños y por lo tanto es difícil trabajar con ellos, fue así entonces que se decidió trabajar con números enteros positivos.
El pH de una disolución se define como el logaritmo negativo de la concentración del ión hidrógeno expresado en (mol/litro), la escala de pH se define por la ecuación:
pH = - log [H+]
El logaritmo negativo proporciona un número positivo para el pH, además el termino [H+] corresponde a la parte numérica de la expresión para la concentración del ión hidrógeno. Debido a que el pH solo es una manera de expresar la concentración del ión hidrógeno, las disoluciones ácidas y básicas (25°C), pueden identificarse por sus valores de pH como sigue:
· Disoluciones acidas: [H+] > 1,0 x 10-7M, pH < 7.00
· Disoluciones básicas: [H+] < 1,0 x 10-7M, pH > 7.00
· Disoluciones neutras: [H+] = 1,0 x 10-7M, pH = 7.00
Se observa que el pH aumenta a medida que el [H+] disminuye.
En el caso del H2O pura, tendremos:
La disociación del H2O es: H2O + H2O ↔ H3O+ + OH-
Por tanto [H3O+] = [OH-] = 1 x 10-7 mol/litro
pH = - log [H3O+]
pH = - log [1 x 10-7]
pH = 7
A 25°C, el pH del agua pura y de cualquier solución acuosa que contenga concentraciones iguales de Ión hidronio y de ión hidroxilo es 7.
Ej: Calcúlese el pH de una solución cuya concentración de ión hidronio es 6,0 x 10 –5 M
pH = - log [6,0 x 10 –5]
= - log [6,0 x 10 –5]
= - [log 6,0 + log 10 –5]
pH = -0,78 + 5 = 4,22
Una escala semejante a la escala del pH puede usarse para expresar la concentración del ión hidroxilo de las soluciones.
El pOH se define como el logaritmo negativo de la concentración molar de iones (OH) es decir:
pOH : - log [OH-]
El pH y el pOH se relacionan así:
[H3O+] [OH-]= 10-14; log [H3O+] [OH-]= log 10-14
Luego log [H3O+] + log [OH-]= - 14 (- log [H3O+])+ (- log [OH-]) = 14
y decir: pH + pOH = 14
| ejemplo_ph_y_poh.docx | |
| File Size: | 21 kb |
| File Type: | docx |
INDICADORES DE pH
Un indicador de pH es una sustancia que permite medir el pH de un medio. Habitualmente, se utilizan como indicador de las sustancias químicas que cambian su color al cambiar el pH de la disolución. El cambio de color se debe a un cambio estructural inducido por laprotonación o desprotonación de la especie. Los indicadores Ácido-base tienen un intervalo de viraje de una unidad arriba y otra abajo de pH, en la que cambian la disolución en la que se encuentran de un color a otro, o de una disolución incolora, a una coloreada.
Los más conocidos son el naranja de metilo, que vira en el intervalo de pH 3,1 - 4,4, de color rojo a naranja, y la fenolftaleína, que vira desde un pH 8 hasta un pH 10, transformando disoluciones incoloras en disoluciones con colores rosados / violetas. Además se pueden usar indicadores caseros como la disolución resultante de hervir con agua col lombarda (repollo colorado), pétalos de rosa roja, raíces de cúrcuma a partir de las cuales se obtiene curcumina, y otros(entre los cuales podemos destacar a la col morada y la piel de ciruela, que son usadas por algunas culturas indígenas).
Los indicadores de pH tienen una constante de protonación, , que informa sobre el desplazamiento de la reacción de protonación de la forma básica del indicador.
Se dice que el cambio de color de un indicador es apreciable cuando la concentración de la forma ácida o de la forma básica es superior o igual a 10 veces la concentración de la forma básica o la forma ácida respectivamente.
Los más conocidos son el naranja de metilo, que vira en el intervalo de pH 3,1 - 4,4, de color rojo a naranja, y la fenolftaleína, que vira desde un pH 8 hasta un pH 10, transformando disoluciones incoloras en disoluciones con colores rosados / violetas. Además se pueden usar indicadores caseros como la disolución resultante de hervir con agua col lombarda (repollo colorado), pétalos de rosa roja, raíces de cúrcuma a partir de las cuales se obtiene curcumina, y otros(entre los cuales podemos destacar a la col morada y la piel de ciruela, que son usadas por algunas culturas indígenas).
Los indicadores de pH tienen una constante de protonación, , que informa sobre el desplazamiento de la reacción de protonación de la forma básica del indicador.
Se dice que el cambio de color de un indicador es apreciable cuando la concentración de la forma ácida o de la forma básica es superior o igual a 10 veces la concentración de la forma básica o la forma ácida respectivamente.
| indicadores_4.docx | |
| File Size: | 29 kb |
| File Type: | docx |
TITULACIÓN DE SOLUCIONES
Neutralización
Recordemos que una reacción de neutralización es aquella en la que un ácido y una base en solución acuosa, interactúan para producir agua y una sal.
Estas reacciones son importantes industrialmente pues constituyen un método eficaz de producir sales de alta pureza.
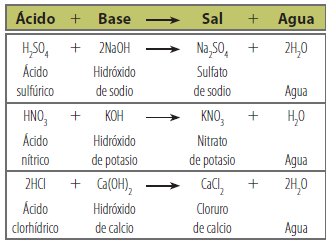
En la tabla se muestran algunos ejemplos de reacciones de neutralización entre diferentes ácidos y bases.
Recordemos que una reacción de neutralización es aquella en la que un ácido y una base en solución acuosa, interactúan para producir agua y una sal.
Estas reacciones son importantes industrialmente pues constituyen un método eficaz de producir sales de alta pureza.
En la tabla se muestran algunos ejemplos de reacciones de neutralización entre diferentes ácidos y bases.
Durante la neutralización, los iones H+ y OH_ reaccionan entre sí para producir agua, al tiempo que los iones restantes, es decir, los pares conjugados del ácido y la base, generan la sal. Sin embargo, por lo general estos iones continúan disociados en solución acuosa, por lo que la sal, como tal, no se forma sino hasta que el agua es retirada, por ejemplo, por evaporación. El pH de la solución luego de que ha ocurrido la neutralización es cercano a la neutralidad, aunque su valor exacto depende de los iones presentes.
QUE ES LA TITULACIÓN
La titulación o valoración de soluciones tiene como principal objetivo determinar la concentración de una solución ácida o básica desconocida, denominada solución analizada. Esto se logra a través de la adición de pequeños volúmenes de una solución ácida o básica de concentración conocida —la solución valorada— a la solución analizada. El proceso se basa en la neutralización que se lleva a cabo entre las dos soluciones, ya que una es ácida y la otra es básica. Así, si sabemos la concentración de iones H+ de la solución valorada, podremos deducir la concentración de iones OH_ en la solución analizada, a partir del volumen de solución valorada usado para neutralizarla, pues la [H+] debe ser igual a la [OH_]. Cuando esto sucede se dice que se ha alcanzado el punto de equivalencia. En este punto, el número de equivalentes-gramo del ácido y la base son iguales. Recordemos que la unidad de concentración más común para ácidos y bases es la normalidad (N), que representa el número de equivalentes-gramo o número de peqg del soluto por litro de solución (N = peqg/L). Para casos en los que las concentraciones son muy bajas se emplean miliequivalentes por mL (meg/mL) para calcular la normalidad.
Para calcular la concentración de la solución analizada debe tenerse en cuenta la igualdad:
NA . VA = NB . VB
En donde:
NA = normalidad del ácido VA = volumen del ácido
NB = normalidad de la base VB = volumen de la base
Es decir, el producto de la normalidad y el volumen del ácido debe ser igual al producto de la normalidad y el volumen de la base.
De igual manera, en cada etapa de la titulación debe cumplirse que:
[H+] . [OH_] = 1,0 x10_14, en la solución analizada.
Determinación de volúmenes en procesos de titulación
Con el fin de aclarar la aplicación de los anteriores conceptos a problemas puntuales, vamos a desarrollar los siguientes problemas.
Para calcular la concentración de la solución analizada debe tenerse en cuenta la igualdad:
NA . VA = NB . VB
En donde:
NA = normalidad del ácido VA = volumen del ácido
NB = normalidad de la base VB = volumen de la base
Es decir, el producto de la normalidad y el volumen del ácido debe ser igual al producto de la normalidad y el volumen de la base.
De igual manera, en cada etapa de la titulación debe cumplirse que:
[H+] . [OH_] = 1,0 x10_14, en la solución analizada.
Determinación de volúmenes en procesos de titulación
Con el fin de aclarar la aplicación de los anteriores conceptos a problemas puntuales, vamos a desarrollar los siguientes problemas.
Curva de titulación
Las curvas de titulación son representaciones del pH en función de la cantidad de solución valorada, añadida a la solución analizada. Son muy útiles para determinar con exactitud el punto de equivalencia y para decidir qué indicador usar para observar más claramente este punto.
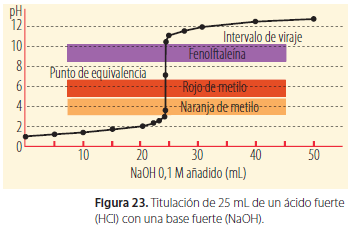
Veamos a manera de ejemplo, la curva de titulación para una solución de HCl de concentración desconocida, valorada con una solución 0,1 M de NaOH, ilustrada en la figura. En ella se observa que, en los extremos de la curva, la variación de pH es suave, con relación a la cantidad de NaOH añadido.
Veamos a manera de ejemplo, la curva de titulación para una solución de HCl de concentración desconocida, valorada con una solución 0,1 M de NaOH, ilustrada en la figura. En ella se observa que, en los extremos de la curva, la variación de pH es suave, con relación a la cantidad de NaOH añadido.
Por el contrario, en las proximidades del punto de equivalencia, para pequeñas cantidades de solución valorada, el pH varía bruscamente. Cualquier indicador cuyo intervalo de viraje esté dentro de este rango de valores de pH (entre 3 y 11) será adecuado para indicar el momento de equivalencia, que corresponde al segmento de la curva con mayor pendiente.
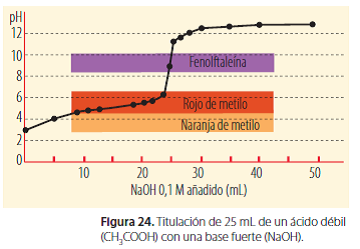
El ejemplo anterior mostraba la titulación de un ácido fuerte con una base fuerte. En la figura se muestra la titulación de un ácido débil (CH3COOH) empleando una base fuerte
(NaOH). Observemos que la pendiente de la curva en las proximidades del punto de equivalencia no es tan pronunciada.
El ejemplo anterior mostraba la titulación de un ácido fuerte con una base fuerte. En la figura se muestra la titulación de un ácido débil (CH3COOH) empleando una base fuerte
(NaOH). Observemos que la pendiente de la curva en las proximidades del punto de equivalencia no es tan pronunciada.
Esto se debe a que en la primera fase de la neutralización, se genera una solución amortiguadora que disminuye las variaciones de pH. También puede verse que el pH en el punto de equivalencia es diferente de 7 (pH 5 8,2), lo cual se relaciona con la presencia del ion acetato (CH3COO_), que se encuentra disociado del ion Na1, una vez se ha completado la neutralización. En este caso la sección de la curva con mayor pendiente se presenta entre pH 6,5 y 11, por lo que el indicador más adecuado para este sistema es la fenolftaleína.
Teoría para las practicas de laboratorio sobre titulaciones e indicadores de pH:
| titulaciones-acido_base.pdf | |
| File Size: | 119 kb |
| File Type: | |
| titulaciones.pdf | |
| File Size: | 167 kb |
| File Type: | |