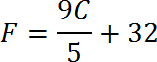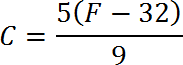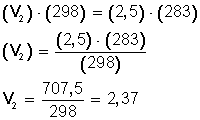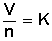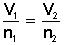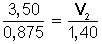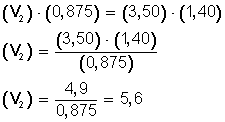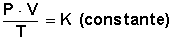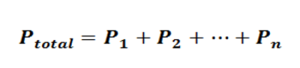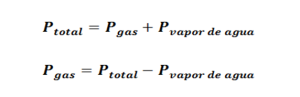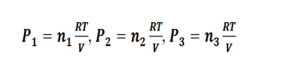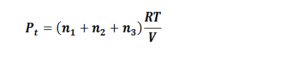En el siguiente enlace encontraras información sobre las leyes de los gases:
LEYES DE LOS GASES
LEYES DE LOS GASES
ESTADO GASEOSO
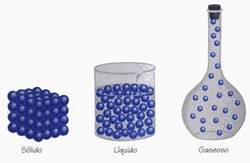
A modo de recordatorio. ¿Cuáles son los estados de la materia?: sólido, líquido y gaseoso, que dependen de la presión y de la temperatura a la que se encuentran sometidos.
En el estado sólido la fuerza de cohesión de las moléculas hace que estas estén muy próximas unas de otros con escaso margen de movimiento entre ellas.
En el estado líquido esta fuerza de cohesión molecular es menor lo cual permite mayor libertad de movimiento entre ellas.
En el estado gaseoso la fuerza de cohesión de las moléculas es muy pequeña, prácticamente nula, lo cual permite que estas se muevan libremente y en todas direcciones.
En este capítulo nos dedicaremos a estudiar este comportamiento de los gases para encontrar una explicación al mismo.
Antes de entrar de lleno en el estudio de las leyes que explican el comportamiento de los gases, veamos cómo influyen en este los eventos físicos que los alteran y que son: temperatura, presión y volumen, además de la cantidad de que se trate.
En el estado sólido la fuerza de cohesión de las moléculas hace que estas estén muy próximas unas de otros con escaso margen de movimiento entre ellas.
En el estado líquido esta fuerza de cohesión molecular es menor lo cual permite mayor libertad de movimiento entre ellas.
En el estado gaseoso la fuerza de cohesión de las moléculas es muy pequeña, prácticamente nula, lo cual permite que estas se muevan libremente y en todas direcciones.
En este capítulo nos dedicaremos a estudiar este comportamiento de los gases para encontrar una explicación al mismo.
Antes de entrar de lleno en el estudio de las leyes que explican el comportamiento de los gases, veamos cómo influyen en este los eventos físicos que los alteran y que son: temperatura, presión y volumen, además de la cantidad de que se trate.

El estudio químico de los gases, generalmente llamados 'aires' empezó a adquirir importancia después de que el fisiólogo británico Stephen Hales desarrollara la cubeta o cuba neumática para recoger y medir el volumen de los gases liberados en un sistema cerrado; los gases eran recogidos sobre el agua tras ser emitidos al calentar diversos sólidos. La cuba neumática se convirtió en un mecanismo valioso para recoger y estudiar gases no contaminados por el aire ordinario. El estudio de los gases avanzó rápidamente y se alcanzó un nuevo nivel de comprensión de los distintos gases.
Esta cubeta permitía recoger y encerrar un gas en un recipiente hermético y después cambiar la presión a que se le sometía, observar el volumen, cambiar la temperatura, convertirlo en líquido, etc.
Esta cubeta permitía recoger y encerrar un gas en un recipiente hermético y después cambiar la presión a que se le sometía, observar el volumen, cambiar la temperatura, convertirlo en líquido, etc.
La interpretación inicial del papel de los gases en la química se produjo en Edimburgo (Escocia) en 1756, cuando Joseph Black publicó sus estudios sobre las reacciones de los carbonatos de magnesio y de calcio. Al calentarlos, estos compuestos desprendían un gas transparente. Ese gas, que hoy llamamos dióxido de carbono, Black lo denominó "aire fijo" y era evidente que tomaba parte en muchas reacciones químicas.
En la década siguiente, el físico británico Henry Cavendish aisló el 'aire inflamable' (hidrógeno). También introdujo el uso del mercurio en lugar del agua como el líquido sobre el que se recogían los gases, posibilitando la recogida de los gases solubles en agua. Esta variante fue utilizada con frecuencia por el químico y teólogo británico Joseph Priestley, quien recogió y estudió casi una docena de gases nuevos. El descubrimiento más importante de Priestley fue el oxígeno; pronto se dio cuenta de que este gas era el componente del aire ordinario responsable de la combustión, y que hacía posible la respiración animal.
Lavoisier, hablando con Priestley en un viaje que este realizó a Paris, entendió rápidamente el significado de esta sustancia, y este hecho abrió el camino para la revolución química que estableció la química moderna. Lavoisier lo llamó 'oxígeno', que significa 'generador de ácidos'.
Tenemos pues que varios científicos estaban estudiando los gases y sus propiedades simultáneamente en varios países de Europa. La atracción de los químicos por los gases estaba causada sobre todo porque a pesar de parecer algo inmaterial sin embargo tenían todas las propiedades de la materia (comenzando por la masa), intervenían de forma crucial en varias muchas reacciones químicas y sobre todo las leyes que se iban descubriendo eran las mismas para todos ellos lo que simplificaba mucho su estudio.
En la década siguiente, el físico británico Henry Cavendish aisló el 'aire inflamable' (hidrógeno). También introdujo el uso del mercurio en lugar del agua como el líquido sobre el que se recogían los gases, posibilitando la recogida de los gases solubles en agua. Esta variante fue utilizada con frecuencia por el químico y teólogo británico Joseph Priestley, quien recogió y estudió casi una docena de gases nuevos. El descubrimiento más importante de Priestley fue el oxígeno; pronto se dio cuenta de que este gas era el componente del aire ordinario responsable de la combustión, y que hacía posible la respiración animal.
Lavoisier, hablando con Priestley en un viaje que este realizó a Paris, entendió rápidamente el significado de esta sustancia, y este hecho abrió el camino para la revolución química que estableció la química moderna. Lavoisier lo llamó 'oxígeno', que significa 'generador de ácidos'.
Tenemos pues que varios científicos estaban estudiando los gases y sus propiedades simultáneamente en varios países de Europa. La atracción de los químicos por los gases estaba causada sobre todo porque a pesar de parecer algo inmaterial sin embargo tenían todas las propiedades de la materia (comenzando por la masa), intervenían de forma crucial en varias muchas reacciones químicas y sobre todo las leyes que se iban descubriendo eran las mismas para todos ellos lo que simplificaba mucho su estudio.
MAGNITUDES QUE DEFINEN UN GAS
Temperatura
La temperatura (T) ejerce gran influencia sobre el estado de las moléculas de un gas aumentando o disminuyendo la velocidad de las mismas. Para trabajar con nuestras fórmulas siempre expresaremos la temperatura en grados Kelvin. Cuando la escala usada esté en grados Celsius, debemos hacer la conversión, sabiendo que 0º C equivale a + 273,15 º Kelvin.
La temperatura (T) ejerce gran influencia sobre el estado de las moléculas de un gas aumentando o disminuyendo la velocidad de las mismas. Para trabajar con nuestras fórmulas siempre expresaremos la temperatura en grados Kelvin. Cuando la escala usada esté en grados Celsius, debemos hacer la conversión, sabiendo que 0º C equivale a + 273,15 º Kelvin.
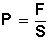
Presión
En Física, presión (P) se define como la relación que existe entre unafuerza (F) y la superficie (S) sobre la que se aplica, y se calcula con la fórmula
Lo cual significa que la Presión (P) es igual a la Fuerza (F) aplicada dividido por la superficie (S) sobre la cual se aplica.
En nuestras fórmulas usaremos como unidad de presión la atmósfera (atm) y el milímetro de mercurio (mmHg), sabiendo que una atmósfera equivale a 760 mmHg O 760 Torr.
La unidad de Presión en el Sistema Internacional es el Pascal.(Pa)otra unidad es la atmósfera =101300 Pa. Otras unidades de presión son:
Kilogramo por centímetro cuadrado Kg/cm2 en ingeniería.
La presión que ejerce la capa de aire sobre la superficie de la tierra se denomina Presión atmosférica y varia según la altura sobre el nivel del mar.
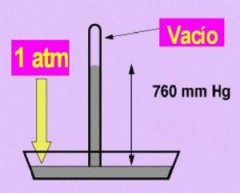
La presión atmosférica se puede medir mediante un aparato llamado barómetro (inventado por Evangelista Torricelli) que consiste en un tubo de vidrio de unos 85 cm de largo, cerrado en uno de sus extremos, lleno de mercurio e invertido sobre un recipiente abierto que contiene también mercurio.
Al invertir el tubo dentro del recipiente, el nivel del mercurio en el tubo desciende hasta cierto punto, indicando la presión ejercida por el mercurio del tubo sobre la superficie del a cubeta ha sido equilibrada exactamente por la presión atmosférica.
Si el experimento se hace a nivel del mar y a 0 grados centígrados, la altura de la columna de Hg es de 76 cm.
La altura de la columna de mercurio dentro del tubo es una medida de la presión atmosférica, ya que la altura de la columna y la presión atmosférica son directamente proporcionales.
1atm= 760 torr / 760 mmHg
1atm= 14.7 lbs/pulg (2)
1atm= 1.033 g/cm2
1atm= 1.103 x10(6) dinas/cm(2)
1 atm = 1.013x10(3) N/m(2) = Pa
En Física, presión (P) se define como la relación que existe entre unafuerza (F) y la superficie (S) sobre la que se aplica, y se calcula con la fórmula
Lo cual significa que la Presión (P) es igual a la Fuerza (F) aplicada dividido por la superficie (S) sobre la cual se aplica.
En nuestras fórmulas usaremos como unidad de presión la atmósfera (atm) y el milímetro de mercurio (mmHg), sabiendo que una atmósfera equivale a 760 mmHg O 760 Torr.
La unidad de Presión en el Sistema Internacional es el Pascal.(Pa)otra unidad es la atmósfera =101300 Pa. Otras unidades de presión son:
Kilogramo por centímetro cuadrado Kg/cm2 en ingeniería.
La presión que ejerce la capa de aire sobre la superficie de la tierra se denomina Presión atmosférica y varia según la altura sobre el nivel del mar.
La presión atmosférica se puede medir mediante un aparato llamado barómetro (inventado por Evangelista Torricelli) que consiste en un tubo de vidrio de unos 85 cm de largo, cerrado en uno de sus extremos, lleno de mercurio e invertido sobre un recipiente abierto que contiene también mercurio.
Al invertir el tubo dentro del recipiente, el nivel del mercurio en el tubo desciende hasta cierto punto, indicando la presión ejercida por el mercurio del tubo sobre la superficie del a cubeta ha sido equilibrada exactamente por la presión atmosférica.
Si el experimento se hace a nivel del mar y a 0 grados centígrados, la altura de la columna de Hg es de 76 cm.
La altura de la columna de mercurio dentro del tubo es una medida de la presión atmosférica, ya que la altura de la columna y la presión atmosférica son directamente proporcionales.
1atm= 760 torr / 760 mmHg
1atm= 14.7 lbs/pulg (2)
1atm= 1.033 g/cm2
1atm= 1.103 x10(6) dinas/cm(2)
1 atm = 1.013x10(3) N/m(2) = Pa
Volumen
Recordemos que volumen es todo el espacio ocupado por algún tipo de materia. En el caso de los gases, estos ocupan todo el volumen disponible del recipiente que los contiene.
Hay muchas unidades para medir el volumen, pero en nuestras fórmulas usaremos el litro (L) y el milílitro (ml). Recordemos que un litro equivale a mil milílitros:
1 L = 1.000 mL
También sabemos que 1 L equivale a 1 decímetro cúbico (1 dm3) o a mil centímetros cúbicos (1.000 cm3) , lo cual hace equivalentes (iguales) 1 mL con 1 cm3:
1 L = 1 dm3 = 1.000 cm3 = 1.000 mL
1 cm3 = 1 mL
Recordemos que volumen es todo el espacio ocupado por algún tipo de materia. En el caso de los gases, estos ocupan todo el volumen disponible del recipiente que los contiene.
Hay muchas unidades para medir el volumen, pero en nuestras fórmulas usaremos el litro (L) y el milílitro (ml). Recordemos que un litro equivale a mil milílitros:
1 L = 1.000 mL
También sabemos que 1 L equivale a 1 decímetro cúbico (1 dm3) o a mil centímetros cúbicos (1.000 cm3) , lo cual hace equivalentes (iguales) 1 mL con 1 cm3:
1 L = 1 dm3 = 1.000 cm3 = 1.000 mL
1 cm3 = 1 mL

Cantidad de gas
Otro parámetro que debe considerarse al estudiar el comportamiento de los gases tiene que ver con la cantidad de un gas la cual se relaciona con el número total de moléculas que la componen.
Para medir la cantidad de un gas usamos como unidad de medida el mol.
Como recordatorio diremos que un mol (ya sea de moléculas o de átomos) es igual a 6,022 por 10 elevado a 23:
1 mol de moléculas = 6,022•1023
1 mol de átomos = 6,022•1023
Recuerden que este número corresponde al llamado número de Avogadro y este nos conduce a una ley llamada, precisamente, ley de Avogadro.
Otro parámetro que debe considerarse al estudiar el comportamiento de los gases tiene que ver con la cantidad de un gas la cual se relaciona con el número total de moléculas que la componen.
Para medir la cantidad de un gas usamos como unidad de medida el mol.
Como recordatorio diremos que un mol (ya sea de moléculas o de átomos) es igual a 6,022 por 10 elevado a 23:
1 mol de moléculas = 6,022•1023
1 mol de átomos = 6,022•1023
Recuerden que este número corresponde al llamado número de Avogadro y este nos conduce a una ley llamada, precisamente, ley de Avogadro.
LEYES DE LOS GASES
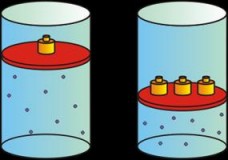
Ley de Boyle
Esta ley nos permite relacionar la presión y el volumen de un gas cuando latemperatura es constante.
La ley de Boyle (conocida también como de Boyle y Mariotte) establece que la presión de un gas en un recipiente cerrado es inversamente proporcional al volumen del recipiente, cuando la temperatura es constante.
Lo cual significa que:
El volumen de un gas es inversamente proporcional a la presión que se le aplica:
En otras palabras:
Si la presión aumenta, el volumen disminuye.
Si la presión disminuye, el volumen aumenta.
Esto nos conduce a que, si la cantidad de gas y la temperatura permanecen constantes, el producto de la presión por el volumen siempre tiene el mismo valor.
Matemáticamente esto es: P . V = K
lo cual significa que el producto de la presión por el volumen es constante.
Para aclarar el concepto:
Tenemos un cierto volumen de gas (V1) que se encuentra a una presión P1. Si variamos la presión a P2, el volumen de gas variará hasta un nuevo valor V2, y se cumplirá:
P1 . V1 = P2 . V2
que es otra manera de expresar la ley de Boyle.
Apliquemos la fórmula en un ejemplo práctico:
Tenemos 4 L de un gas que están a 600 mmHg de presión. ¿Cuál será su volumen si aumentamos la presión hasta 800 mmHg? La temperatura es constante, no varía.
Solución:
Como los datos de presión están ambos en milímetros de mercurio (mmHg) no es necesario hacer la conversión a atmósferas (atm). Si solo uno de ellos estuviera en mmHg y el otro en atm, habría que dejar los dos en atm.
Aclarado esto, sustituimos los valores en la ecuación P1V1 = P2V2.
(600 mmHg) . (4L) = (800 mmHg) . (V2)
Despejamos V2:
V2 = (600 mmHg) . (4L) / (800 mmHg)
V2 = 3L
Respuesta:
Si aumentamos la presión hasta 800 mmHg el volumen disminuye hasta llegar a los 3 L.
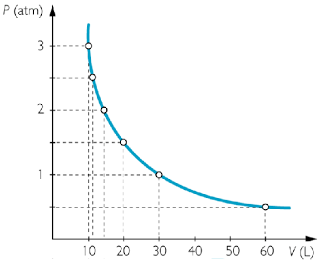
Si tuviéramos un manómetro para medir presiones, y el recipiente fuera más grande, hubiéramos obtenido la siguiente gráfica.
Esta ley nos permite relacionar la presión y el volumen de un gas cuando latemperatura es constante.
La ley de Boyle (conocida también como de Boyle y Mariotte) establece que la presión de un gas en un recipiente cerrado es inversamente proporcional al volumen del recipiente, cuando la temperatura es constante.
Lo cual significa que:
El volumen de un gas es inversamente proporcional a la presión que se le aplica:
En otras palabras:
Si la presión aumenta, el volumen disminuye.
Si la presión disminuye, el volumen aumenta.
Esto nos conduce a que, si la cantidad de gas y la temperatura permanecen constantes, el producto de la presión por el volumen siempre tiene el mismo valor.
Matemáticamente esto es: P . V = K
lo cual significa que el producto de la presión por el volumen es constante.
Para aclarar el concepto:
Tenemos un cierto volumen de gas (V1) que se encuentra a una presión P1. Si variamos la presión a P2, el volumen de gas variará hasta un nuevo valor V2, y se cumplirá:
P1 . V1 = P2 . V2
que es otra manera de expresar la ley de Boyle.
Apliquemos la fórmula en un ejemplo práctico:
Tenemos 4 L de un gas que están a 600 mmHg de presión. ¿Cuál será su volumen si aumentamos la presión hasta 800 mmHg? La temperatura es constante, no varía.
Solución:
Como los datos de presión están ambos en milímetros de mercurio (mmHg) no es necesario hacer la conversión a atmósferas (atm). Si solo uno de ellos estuviera en mmHg y el otro en atm, habría que dejar los dos en atm.
Aclarado esto, sustituimos los valores en la ecuación P1V1 = P2V2.
(600 mmHg) . (4L) = (800 mmHg) . (V2)
Despejamos V2:
V2 = (600 mmHg) . (4L) / (800 mmHg)
V2 = 3L
Respuesta:
Si aumentamos la presión hasta 800 mmHg el volumen disminuye hasta llegar a los 3 L.
Si tuviéramos un manómetro para medir presiones, y el recipiente fuera más grande, hubiéramos obtenido la siguiente gráfica.
Realiza una gráfica p/V con el volumen en ordenadas.
Observamos que p y V son inversamente proporcionales y están relacionados por una expresión del tipo p.V=cte
Al aumentar el volumen, las partículas (átomos o moléculas) del gas tardan más en llegar a las paredes del recipiente y por lo tanto chocan menos veces por unidad de tiempo contra ellas. Esto significa que la presión será menor ya que ésta representa la frecuencia de choques del gas contra las paredes.
Cuando disminuye el volumen la distancia que tienen que recorrer las partículas es menor y por tanto se producen más choques en cada unidad de tiempo: aumenta la presión.
Lo que Boyle descubrió es que si la cantidad de gas y la temperatura permanecen constantes, el producto de la presión por el volumen siempre tiene el mismo valor.
Observamos que p y V son inversamente proporcionales y están relacionados por una expresión del tipo p.V=cte
Al aumentar el volumen, las partículas (átomos o moléculas) del gas tardan más en llegar a las paredes del recipiente y por lo tanto chocan menos veces por unidad de tiempo contra ellas. Esto significa que la presión será menor ya que ésta representa la frecuencia de choques del gas contra las paredes.
Cuando disminuye el volumen la distancia que tienen que recorrer las partículas es menor y por tanto se producen más choques en cada unidad de tiempo: aumenta la presión.
Lo que Boyle descubrió es que si la cantidad de gas y la temperatura permanecen constantes, el producto de la presión por el volumen siempre tiene el mismo valor.
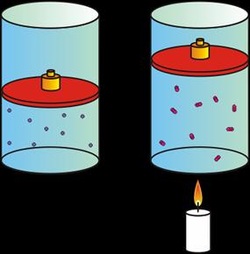
Ley de Charles
Mediante esta ley relacionamos la temperatura y el volumen de un gas cuando mantenemos la presión constante.
Textualmente, la ley afirma que:
El volumen de un gas es directamente proporcional a la temperatura del gas.
En otras palabras:
Si aumenta la temperatura aplicada al gas, el volumen del gas aumenta.
Si disminuye la temperatura aplicada al gas, el volumen del gas disminuye.
Como lo descubrió Charles, si la cantidad de gas y la presión permanecen constantes, el cociente entre el volumen (V) y la temperatura (T) siempre tiene el mismo valor (K) (es constante).
Matemáticamente esto se expresa en la fórmula V / T = K
lo cual significa que el cociente entre el volumen y la temperatura es constante.
Intentemos ejemplificar:
Supongamos que tenemos un cierto volumen de gas V1 que se encuentra a una temperatura T1. Si aumentamos la temperatura a T2 el volumen del gas aumentará hasta V2, y se cumplirá que:
V1 /T1 = V2 / T2
que es otra manera de expresar la ley de Charles.
Veamos un ejemplo práctico y sencillo:
Un gas cuya temperatura llega a 25° C tiene un volumen de 2,5 L. Para experimentar, bajamos la temperatura a 10° C ¿Cuál será su nuevo volumen?
Solución:
El primer paso es recordar que en todas estas fórmulas referidas a la temperatura hay que usar siempre la escala Kelvin.
Por lo tanto, lo primero es expresar la temperatura en grados Kelvin:
T1 = (25 + 273) K= 298 K
T2 = (10 + 273 ) K= 283 K
Ahora, sustituimos los datos en la ecuación: V1 /T1 = V2 / T2
2.5 L / 298 K = V2 / 283 K
Ahora, despejamos V2:
Respuesta:
Si bajamos la temperatura hasta los 10º C (283º K) el nuevo volumen del gas será 2,37 L.
Mediante esta ley relacionamos la temperatura y el volumen de un gas cuando mantenemos la presión constante.
Textualmente, la ley afirma que:
El volumen de un gas es directamente proporcional a la temperatura del gas.
En otras palabras:
Si aumenta la temperatura aplicada al gas, el volumen del gas aumenta.
Si disminuye la temperatura aplicada al gas, el volumen del gas disminuye.
Como lo descubrió Charles, si la cantidad de gas y la presión permanecen constantes, el cociente entre el volumen (V) y la temperatura (T) siempre tiene el mismo valor (K) (es constante).
Matemáticamente esto se expresa en la fórmula V / T = K
lo cual significa que el cociente entre el volumen y la temperatura es constante.
Intentemos ejemplificar:
Supongamos que tenemos un cierto volumen de gas V1 que se encuentra a una temperatura T1. Si aumentamos la temperatura a T2 el volumen del gas aumentará hasta V2, y se cumplirá que:
V1 /T1 = V2 / T2
que es otra manera de expresar la ley de Charles.
Veamos un ejemplo práctico y sencillo:
Un gas cuya temperatura llega a 25° C tiene un volumen de 2,5 L. Para experimentar, bajamos la temperatura a 10° C ¿Cuál será su nuevo volumen?
Solución:
El primer paso es recordar que en todas estas fórmulas referidas a la temperatura hay que usar siempre la escala Kelvin.
Por lo tanto, lo primero es expresar la temperatura en grados Kelvin:
T1 = (25 + 273) K= 298 K
T2 = (10 + 273 ) K= 283 K
Ahora, sustituimos los datos en la ecuación: V1 /T1 = V2 / T2
2.5 L / 298 K = V2 / 283 K
Ahora, despejamos V2:
Respuesta:
Si bajamos la temperatura hasta los 10º C (283º K) el nuevo volumen del gas será 2,37 L.
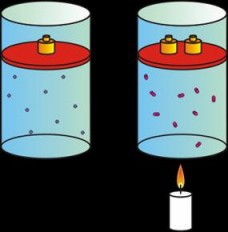
Ley de Gay-Lussac
Esta ley establece la relación entre la presión (P) y la temperatura (T) de un gas cuando el volumen (V) se mantiene constante, y dice textualmente:
La presión del gas es directamente proporcional a su temperatura.
Esto significa que:
Si aumentamos la temperatura, aumentará la presión.
Si disminuimos la temperatura, disminuirá la presión.
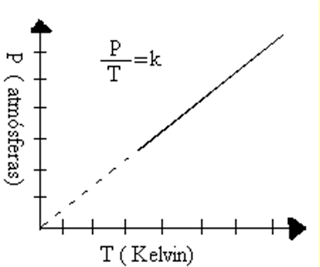
Si lo llevamos al plano matemático, esto queda demostrado con la siguiente ecuación:
P / T = K
la cual nos indica que el cociente entre la presión y la temperatura siempre tiene el mismo valor; es decir, es constante.
Llevemos esto a la práctica y supongamos que tenemos un gas, cuyo volumen (V) no varía, a una presión P1 y a una temperatura T1. Para experimentar, variamos la temperatura hasta un nuevo valor T2, entonces la presión cambiará a P2, y tendrá que cumplirse la siguiente ecuación:
P1 / T1 = P2 / T2
que es la misma Ley de Gay-Lussac expresada de otra forma.
Debemos recordar, además, que esta ley, al igual que la de Charles, está expresada en función de la temperatura absoluta, y tal como en la Ley de Charles, las temperaturas han de expresarse en grados Kelvin.
Veamos un ejemplo:
Tenemos un cierto volumen de un gas bajo una presión de 970 mmHg cuando su temperatura es de 25° C. ¿A qué temperatura deberá estar para que su presión sea 760 mmHg?
Solución:
Lo primero que debemos hacer es convertir los 25º C a grados Kelvin:
T1 = (25 + 273) K= 298 K
Ahora sustituimos los datos en la ecuación:
P1 / T1 = P2 / T2
970 mmHg / 298 K = 760 mmHg / T2
Ahora despejamos T2:
T2 = (298 K) . (760 mmHg) / (970 mmHg)
T2 = 233,5 K
Respuesta:
La temperatura debe bajar hasta los 233,5º Kelvin. Si convertimos estos grados en grados Celsius hacemos
233,5 − 273 = −39,5 °C.
Esta ley establece la relación entre la presión (P) y la temperatura (T) de un gas cuando el volumen (V) se mantiene constante, y dice textualmente:
La presión del gas es directamente proporcional a su temperatura.
Esto significa que:
Si aumentamos la temperatura, aumentará la presión.
Si disminuimos la temperatura, disminuirá la presión.
Si lo llevamos al plano matemático, esto queda demostrado con la siguiente ecuación:
P / T = K
la cual nos indica que el cociente entre la presión y la temperatura siempre tiene el mismo valor; es decir, es constante.
Llevemos esto a la práctica y supongamos que tenemos un gas, cuyo volumen (V) no varía, a una presión P1 y a una temperatura T1. Para experimentar, variamos la temperatura hasta un nuevo valor T2, entonces la presión cambiará a P2, y tendrá que cumplirse la siguiente ecuación:
P1 / T1 = P2 / T2
que es la misma Ley de Gay-Lussac expresada de otra forma.
Debemos recordar, además, que esta ley, al igual que la de Charles, está expresada en función de la temperatura absoluta, y tal como en la Ley de Charles, las temperaturas han de expresarse en grados Kelvin.
Veamos un ejemplo:
Tenemos un cierto volumen de un gas bajo una presión de 970 mmHg cuando su temperatura es de 25° C. ¿A qué temperatura deberá estar para que su presión sea 760 mmHg?
Solución:
Lo primero que debemos hacer es convertir los 25º C a grados Kelvin:
T1 = (25 + 273) K= 298 K
Ahora sustituimos los datos en la ecuación:
P1 / T1 = P2 / T2
970 mmHg / 298 K = 760 mmHg / T2
Ahora despejamos T2:
T2 = (298 K) . (760 mmHg) / (970 mmHg)
T2 = 233,5 K
Respuesta:
La temperatura debe bajar hasta los 233,5º Kelvin. Si convertimos estos grados en grados Celsius hacemos
233,5 − 273 = −39,5 °C.
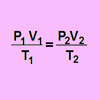
RESUMEN DE LAS LEYES DE LOS GASES
En un gas encerrado en un recipiente se cumple que la expresión p.V/T es constante. Esta constante es evidente que depende de la cantidad de gas. Si aumentamos la cantidad de gas p.V/T aumenta.
En un gas encerrado en un recipiente se cumple que la expresión p.V/T es constante. Esta constante es evidente que depende de la cantidad de gas. Si aumentamos la cantidad de gas p.V/T aumenta.
LEY DE AVOGADRO
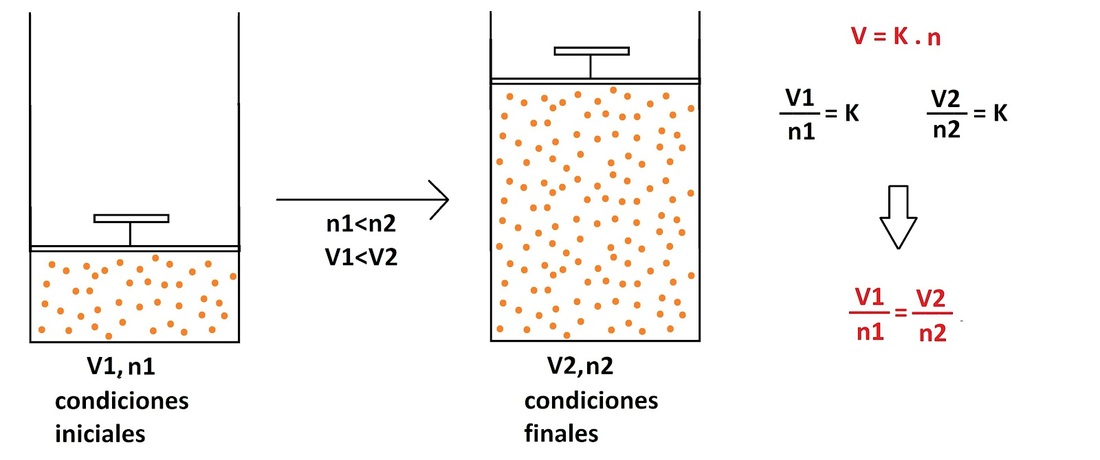
Esta ley relaciona la cantidad de gas (n, en moles) con su volumen en litros (L), considerando que la presión y la temperatura permanecen constantes (no varían).
El enunciado de la ley dice que:
El volumen de un gas es directamente proporcional a la cantidad del mismo.
Esto significa que:
Si aumentamos la cantidad de gas, aumentará el volumen del mismo.
Si disminuimos la cantidad de gas, disminuirá el volumen del mismo.
Esto tan simple, podemos expresarlo en términos matemáticos con la siguiente fórmula:
Que se traduce en que si dividimos el volumen de un gas por el número de moles que lo conforman obtendremos un valor constante.
Esta ley relaciona la cantidad de gas (n, en moles) con su volumen en litros (L), considerando que la presión y la temperatura permanecen constantes (no varían).
El enunciado de la ley dice que:
El volumen de un gas es directamente proporcional a la cantidad del mismo.
Esto significa que:
Si aumentamos la cantidad de gas, aumentará el volumen del mismo.
Si disminuimos la cantidad de gas, disminuirá el volumen del mismo.
Esto tan simple, podemos expresarlo en términos matemáticos con la siguiente fórmula:
Que se traduce en que si dividimos el volumen de un gas por el número de moles que lo conforman obtendremos un valor constante.
Tan simple como: más gas, mayor volumen.
Esto debido a que si ponemos más moles (cantidad de moléculas) de un gas en un recipiente tendremos, obviamente, más gas (más volumen), así de simple.
Esto se expresa en la ecuación:
Esto debido a que si ponemos más moles (cantidad de moléculas) de un gas en un recipiente tendremos, obviamente, más gas (más volumen), así de simple.
Esto se expresa en la ecuación:
Veamos un ejemplo práctico y sencillo:
Tenemos 3,50 L de un gas que, sabemos, corresponde a 0,875 mol. Inyectamos gas al recipiente hasta llegar a 1,40 mol, ¿cuál será el nuevo volumen del gas? (la temperatura y la presión las mantenemos constantes).
Solución:
Aplicamos la ecuación de la ley de Avogadro:
Tenemos 3,50 L de un gas que, sabemos, corresponde a 0,875 mol. Inyectamos gas al recipiente hasta llegar a 1,40 mol, ¿cuál será el nuevo volumen del gas? (la temperatura y la presión las mantenemos constantes).
Solución:
Aplicamos la ecuación de la ley de Avogadro:
Reemplazamos los valores correspondientes.
Ahora, despejamos V2, para ello, pasamos completo a la izquierda el miembro con la incógnita (V2)
Respuesta:
El nuevo volumen (V2), ya que aumentamos los moles hasta 1,40 (n2), es ahora 5,6 L
Ahora, despejamos V2, para ello, pasamos completo a la izquierda el miembro con la incógnita (V2)
Respuesta:
El nuevo volumen (V2), ya que aumentamos los moles hasta 1,40 (n2), es ahora 5,6 L
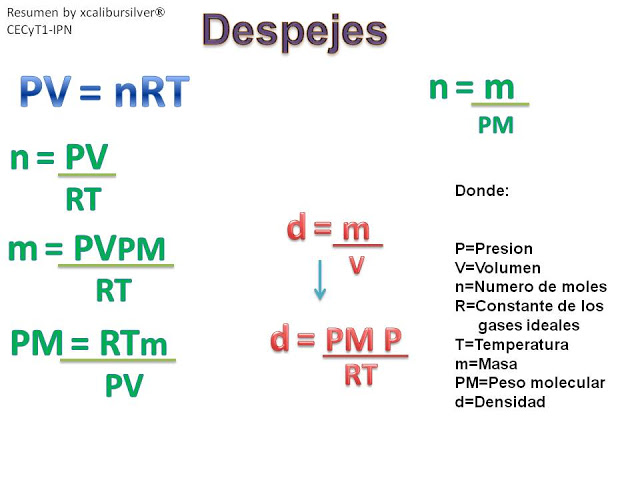
LEY GENERAL DE LOS GASES O ECUACIÓN GENERAL DE LOS GASES
Las leyes parciales analizada precedentemente pueden combinarse y obtener una ley o ecuación que relaciones todas las variables al mismo tiempo.
Según esta ecuación o ley general:
Según esta ecuación o ley general:
Esto significa que, si tenemos una cantidad fija de gas y sobre la misma variamos las condiciones de presión (P), volumen (V) o temperatura (T) el resultado de aplicar esta fórmula con diferentes valores, será una constante.
Veamos un ejemplo, para aclarar:
Supongamos que tenemos una cierta cantidad fija de un gas (n1), que está a una presión (P1), ocupando un volumen (V1) a una temperatura (T1).
Estas variables se relacionan entre sí cumpliendo con la siguiente ecuación:
Donde R es una constante universal conocida ya que se puede determinar en forma experimental.
Veamos un ejemplo, para aclarar:
Supongamos que tenemos una cierta cantidad fija de un gas (n1), que está a una presión (P1), ocupando un volumen (V1) a una temperatura (T1).
Estas variables se relacionan entre sí cumpliendo con la siguiente ecuación:
Donde R es una constante universal conocida ya que se puede determinar en forma experimental.
Algo para recordar y utilizar:
Cuando se dice que dos elementos o cantidades son inversamente proporcionales, deben multiplicarse entre sí cada vez que sus valores varían y el resultado tiene que ser siempre el mismo (constante).
Ahora, cuando dos elementos o cantidades son directamente proporcionales, deben dividirse entre sí cada vez que sus valores varían y el resultado tiene que ser siempre el mismo (constante).
Cuando se dice que dos elementos o cantidades son inversamente proporcionales, deben multiplicarse entre sí cada vez que sus valores varían y el resultado tiene que ser siempre el mismo (constante).
Ahora, cuando dos elementos o cantidades son directamente proporcionales, deben dividirse entre sí cada vez que sus valores varían y el resultado tiene que ser siempre el mismo (constante).
LEY DE LAS PRESIONES PARCIALES O LEY DE DALTON
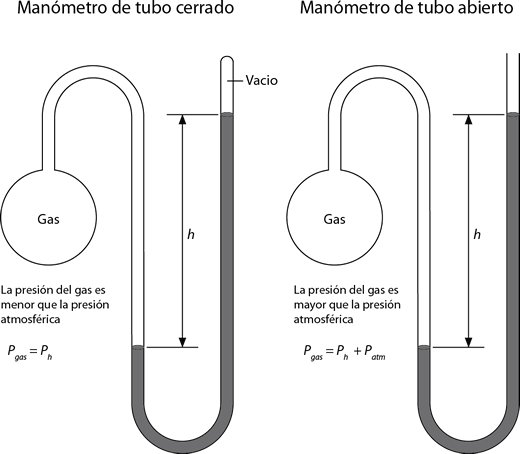
Cuando se colocan en un recipiente varios gases que no reaccionan entre sí, las partículas de cada gas chocan contra las paredes del recipiente, independientemente de la presencia de los otros gases.
Esta ley dice: “la presión total de una mezcla gaseosa es igual a la suma de las presiones parciales de los gases que la componen” figura 1
Esta ley dice: “la presión total de una mezcla gaseosa es igual a la suma de las presiones parciales de los gases que la componen” figura 1
La mayoría de los gases son insolubles al agua, por lo que en el laboratorio se obtienen fácilmente con el método de desplazamiento del agua. Por tanto para calcular la presión del gas seco, es necesario conocer la presión del vapor de agua a esa temperatura. figura 2
La presión que ejerce un gas es proporcional al número de moléculas presentes en el gas, e independientemente de su naturaleza. En una mezcla gaseosa cada uno de los gases obedece la ecuación del gas ideal, por lo tanto: figura 3
Si todos los gases se encuentran en las mismas condiciones de volumen y temperatura, tenemos: figura 4
La presión que ejerce un gas es proporcional al número de moléculas presentes en el gas, e independientemente de su naturaleza. En una mezcla gaseosa cada uno de los gases obedece la ecuación del gas ideal, por lo tanto: figura 3
Si todos los gases se encuentran en las mismas condiciones de volumen y temperatura, tenemos: figura 4
| presiones_parciales_ley_de_dalton.pdf | |
| File Size: | 148 kb |
| File Type: | |
LEY DE DIFUSION DE LOS GASES O LEY DE GRAHAM
| ley_difusion_gases.pdf | |
| File Size: | 50 kb |
| File Type: | |