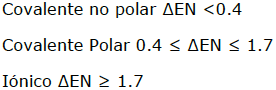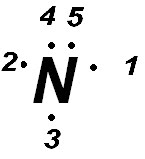CONCEPTO DE ENLACE QUÍMICO
Los enlaces químicos (determinados por la manera en la cual se comportan los electrones), dentro de la física, son fuerzas que permiten la unión de los átomos, para constituir moléculas, que poseen mayor estabilidad; dos átomos ligados a través de alguno de estos enlaces, conforman una molécula. La mayoría de los átomos logra ser considerado estable, cuando posee ocho electrones en su último nivel energético (regla del octeto).
En los enlacen químicos tienen gran influencia el estado de oxidación y la electronegatividad de los elementos que van a unirse. El estado de oxidación indica la carga eléctrica del ión (átomo cargado eléctricamente), que puede ser positiva (catión) o negativa (anión); y expresa el comportamiento de los electrones en las uniones químicas. La electronegatividad es la fuerza que posee cada átomo, para atraer los electrones del mismo, y de otros átomos; esto define en gran medida el tipo de enlace que se formará entre dos átomos determinados.
Existen diferentes tipos de enlaces químicos; entre ellos encontramos a: los enlaces covalentes y los enlaces iónicos (enlaces fuertes), y los puentes de hidrógeno y las fuerzas de Van der Waals (enlaces débiles).
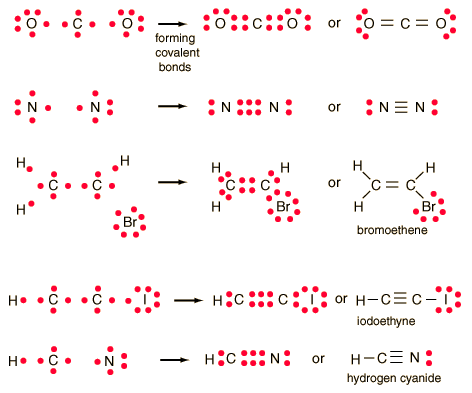
En los enlaces covalentes, que son fuertes y estables, se comparten uno o más pares de electrones (hallados en el último orbital del átomo) entre dos o más átomos, de elementos no metales.
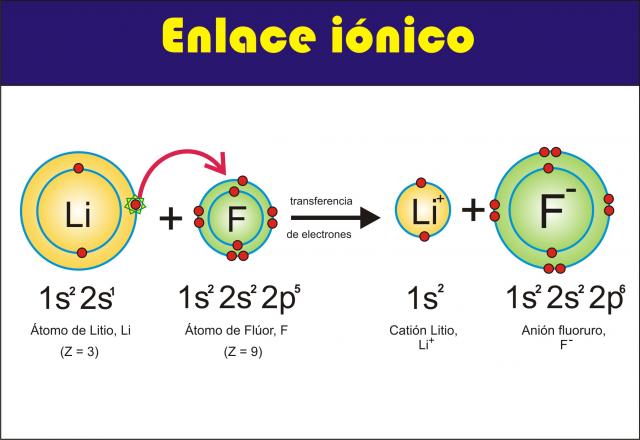
Los enlaces iónicos se caracterizan por la transferencia de electrones entre elementos metales y no metales; el metal tiende a ceder electrones, mientras que el no metal tiende a ganar electrones.
Los enlaces mediante puentes de hidrógeno son débiles, no obstante, cuando se forman muchos de estos enlaces, adquieren una fuerza mayor, y logran tener una influencia notoria en las sustancias, respecto de su estructura y propiedades. Los enlaces por puentes de hidrógeno se forman por la unión entre un átomo electronegativo y un hidrógeno, unido de manera covalente a otro átomo electronegativo distinto.
Las fuerzas de Van der Waals son un tipo de enlace químico débil y breve (pero aditivo), que surge entre átomos (de moléculas no polares) que se encuentran cerca unos de otros, y son útiles para el mantenimiento de las estructuras de diversas sustancias valiosas.
En los enlacen químicos tienen gran influencia el estado de oxidación y la electronegatividad de los elementos que van a unirse. El estado de oxidación indica la carga eléctrica del ión (átomo cargado eléctricamente), que puede ser positiva (catión) o negativa (anión); y expresa el comportamiento de los electrones en las uniones químicas. La electronegatividad es la fuerza que posee cada átomo, para atraer los electrones del mismo, y de otros átomos; esto define en gran medida el tipo de enlace que se formará entre dos átomos determinados.
Existen diferentes tipos de enlaces químicos; entre ellos encontramos a: los enlaces covalentes y los enlaces iónicos (enlaces fuertes), y los puentes de hidrógeno y las fuerzas de Van der Waals (enlaces débiles).
En los enlaces covalentes, que son fuertes y estables, se comparten uno o más pares de electrones (hallados en el último orbital del átomo) entre dos o más átomos, de elementos no metales.
Los enlaces iónicos se caracterizan por la transferencia de electrones entre elementos metales y no metales; el metal tiende a ceder electrones, mientras que el no metal tiende a ganar electrones.
Los enlaces mediante puentes de hidrógeno son débiles, no obstante, cuando se forman muchos de estos enlaces, adquieren una fuerza mayor, y logran tener una influencia notoria en las sustancias, respecto de su estructura y propiedades. Los enlaces por puentes de hidrógeno se forman por la unión entre un átomo electronegativo y un hidrógeno, unido de manera covalente a otro átomo electronegativo distinto.
Las fuerzas de Van der Waals son un tipo de enlace químico débil y breve (pero aditivo), que surge entre átomos (de moléculas no polares) que se encuentran cerca unos de otros, y son útiles para el mantenimiento de las estructuras de diversas sustancias valiosas.
REGLA DEL OCTETO
La regla del octeto establece que los átomos de los elementos se enlazan unos a otros en el intento de completar su capa de valencia (ultima capa de la electrosfera).
La denominación “regla del octeto” surgió en razón de la cantidad establecida de electrones para la estabilidad de un elemento, o sea, el átomo queda estable cuando presenta en su capa de valencia 8 electrones.
Para alcanzar tal estabilidad sugerida por la regla del octeto, cada elemento precisa ganar o perder (compartir) electrones en los enlaces químicos, de esa forma ellos adquieren ocho electrones en la capa de valencia.Esta regla indica que cuando se van a enlazar dos átomos iguales, los electrones de valencia de éstos se organizan de tal manera que, al formar el enlace por compartición de pares de electrones, cada uno de los átomos al final adopta una estructura de gas noble, quedando ambos rodeados de 8 electrones en sus últimos niveles de energía. Cuando se trata de átomos diferentes, el elemento más electronegativo o no metálico es el que se rodea de ocho electrones.
Esta Regla tiene algunas excepciones como es el caso de que no se aplica en la formación de enlaces con pares de átomos de hidrógeno.
Por ejemplo tenemos:
La denominación “regla del octeto” surgió en razón de la cantidad establecida de electrones para la estabilidad de un elemento, o sea, el átomo queda estable cuando presenta en su capa de valencia 8 electrones.
Para alcanzar tal estabilidad sugerida por la regla del octeto, cada elemento precisa ganar o perder (compartir) electrones en los enlaces químicos, de esa forma ellos adquieren ocho electrones en la capa de valencia.Esta regla indica que cuando se van a enlazar dos átomos iguales, los electrones de valencia de éstos se organizan de tal manera que, al formar el enlace por compartición de pares de electrones, cada uno de los átomos al final adopta una estructura de gas noble, quedando ambos rodeados de 8 electrones en sus últimos niveles de energía. Cuando se trata de átomos diferentes, el elemento más electronegativo o no metálico es el que se rodea de ocho electrones.
Esta Regla tiene algunas excepciones como es el caso de que no se aplica en la formación de enlaces con pares de átomos de hidrógeno.
Por ejemplo tenemos:
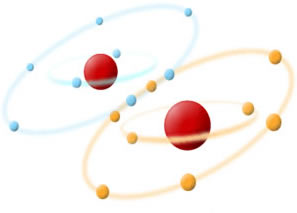
Veamos que los átomos de oxígeno se enlazan para alcanzar la estabilidad sugerida por la regla del octeto. Los diferentes colores de electrosfera mostrados en la figura nos ayudan a interpretar lo siguiente:
1 – Átomos de Oxigeno poseen seis electrones en la capa de valencia (anillo externo en la figura)
2 – Para volverse estables precisan contar con ocho electrones. ¿Y como lo logran entonces?
Comparten dos electrones (indicado en la unión de los dos anillos), formando una molécula de gas oxígeno (O2)
La justificativa para esta regla es que las moléculas o iones, tienden a ser más estables cuando la capa de electrones externa de cada uno de sus átomos está llena con ocho electrones (configuración de un gas noble).
Es por ello que los elementos tienden siempre a formar enlaces en la busqueda de tal estabilidad.
Excepciones a la regla del Octeto
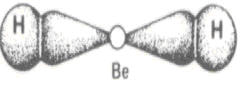
Berilio (Be)
Es una excepción a la regla del Octeto porque es capaz de formar compuestos con dos enlaces simples, siendo así, se estabiliza con apenas cuatro electrones en la capa de valencia.
1 – Átomos de Oxigeno poseen seis electrones en la capa de valencia (anillo externo en la figura)
2 – Para volverse estables precisan contar con ocho electrones. ¿Y como lo logran entonces?
Comparten dos electrones (indicado en la unión de los dos anillos), formando una molécula de gas oxígeno (O2)
La justificativa para esta regla es que las moléculas o iones, tienden a ser más estables cuando la capa de electrones externa de cada uno de sus átomos está llena con ocho electrones (configuración de un gas noble).
Es por ello que los elementos tienden siempre a formar enlaces en la busqueda de tal estabilidad.
Excepciones a la regla del Octeto
Berilio (Be)
Es una excepción a la regla del Octeto porque es capaz de formar compuestos con dos enlaces simples, siendo así, se estabiliza con apenas cuatro electrones en la capa de valencia.
Como el hidrógeno (H) precisa ceder dos electrones para realizar el enlace (H ― Be ― H), el átomo de Berilio (Be) comparte sus electrones y alcanza la estabilidad.
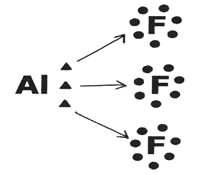
Aluminio (Al)
Es una excepción a la regla del octeto porque alcanza la estabilidad con seis electrones en la capa de valencia. El átomo de aluminio tiende a donar sus electrones y así puede formar tres enlaces simples con otros átomos
En este caso, el Aluminio (Al) formó tres enlaces con tres átomos de Fluor (F)
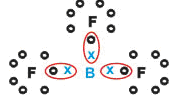
Boro (B)
Forma sustancias moleculares con tres enlaces simples.
Fijémonos que el Boro (B) tiene la tendencia de donar sus electrones para los átomos de Flúor (F), este si obedece a la regla del Octeto, necesitando sus ocho electrones en la capa de valencia. Como el Boro cede sus electrones, el Flúor se estabiliza con el Octeto formado.
Aluminio (Al)
Es una excepción a la regla del octeto porque alcanza la estabilidad con seis electrones en la capa de valencia. El átomo de aluminio tiende a donar sus electrones y así puede formar tres enlaces simples con otros átomos
En este caso, el Aluminio (Al) formó tres enlaces con tres átomos de Fluor (F)
Boro (B)
Forma sustancias moleculares con tres enlaces simples.
Fijémonos que el Boro (B) tiene la tendencia de donar sus electrones para los átomos de Flúor (F), este si obedece a la regla del Octeto, necesitando sus ocho electrones en la capa de valencia. Como el Boro cede sus electrones, el Flúor se estabiliza con el Octeto formado.
Aplicación de la regla del octeto con átomos de elementos diferentes:
LA ELECTRONEGATIVIDAD
La electronegatividad de un elemento mide su tendencia a atraer hacia sí electrones, cuando está químicamente combinado con otro átomo. Cuanto mayor sea, mayor será su capacidad para atraerlos.
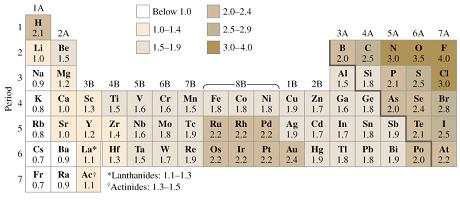
Pauling la definió como la capacidad de un átomo en una molécula para atraer electrones hacia así. Sus valores, basados en datos termoquímicos, han sido determinados en una escala arbitraria, denominada escala de Pauling, cuyo valor máximo es 4 que es el valor asignado al flúor, el elemento más electronegativo. El elemento menos electronegativo, el cesio, tiene una electronegatividad de 0,7.
La electronegatividad de un átomo en una molécula está relacionada con su potencial de ionización y su electroafinidad.
Un átomo con una afinidad electrónica muy negativa y un potencial de ionización elevado, atraerá electrones de otros átomos y además se resistirá a dejar ir sus electrones ante atracciones externas; será muy electronegativo.
El método sugerido por el profesor R.S. Mulliken promedia los valores del potencial de ionización y afinidad electrónica de un elemento:
XM = 0,0085 (P.I. + A.E.)
Variación periódica
· Las electronegatividades de los elementos representativos aumentan de izquierda a derecha a lo largo de los periodos y de abajo a arriba dentro de cada grupo.
· Las variaciones de electronegatividades de los elementos de transición no son tan regulares. En general, las energías de ionización y las electronegatividades son inferiores para los elementos de la zona inferior izquierda de la tabla periódica que para los de la zona superior derecha.
El concepto de la electronegatividad es muy útil para conocer el tipo de enlace que originarán dos átomos en su unión:
El enlace entre átomos de la misma clase y de la misma electronegatividad es apolar.
Cuanto mayores sean las diferencias de electronegatividad entre dos átomos tanto mayor será la densidad electrónica del orbital molecular en las proximidades del átomo más electronegativo. Se origina un enlace polar.
Cuando la diferencia de electronegatividades es suficientemente alta, se produce una transferencia completa de electrones, dando lugar a la formación de especies iónicas.
Cuando se enlazan dos átomos iguales, con la misma electronegatividad, la diferencia es cero, y el enlace es covalente no polar, ya que los electrones son atraídos por igual por ambos átomos.
El criterio que se sigue para determinar el tipo de enlace a partir de la diferencia de electronegativad, en términos, generales es el siguiente:
Pauling la definió como la capacidad de un átomo en una molécula para atraer electrones hacia así. Sus valores, basados en datos termoquímicos, han sido determinados en una escala arbitraria, denominada escala de Pauling, cuyo valor máximo es 4 que es el valor asignado al flúor, el elemento más electronegativo. El elemento menos electronegativo, el cesio, tiene una electronegatividad de 0,7.
La electronegatividad de un átomo en una molécula está relacionada con su potencial de ionización y su electroafinidad.
Un átomo con una afinidad electrónica muy negativa y un potencial de ionización elevado, atraerá electrones de otros átomos y además se resistirá a dejar ir sus electrones ante atracciones externas; será muy electronegativo.
El método sugerido por el profesor R.S. Mulliken promedia los valores del potencial de ionización y afinidad electrónica de un elemento:
XM = 0,0085 (P.I. + A.E.)
Variación periódica
· Las electronegatividades de los elementos representativos aumentan de izquierda a derecha a lo largo de los periodos y de abajo a arriba dentro de cada grupo.
· Las variaciones de electronegatividades de los elementos de transición no son tan regulares. En general, las energías de ionización y las electronegatividades son inferiores para los elementos de la zona inferior izquierda de la tabla periódica que para los de la zona superior derecha.
El concepto de la electronegatividad es muy útil para conocer el tipo de enlace que originarán dos átomos en su unión:
El enlace entre átomos de la misma clase y de la misma electronegatividad es apolar.
Cuanto mayores sean las diferencias de electronegatividad entre dos átomos tanto mayor será la densidad electrónica del orbital molecular en las proximidades del átomo más electronegativo. Se origina un enlace polar.
Cuando la diferencia de electronegatividades es suficientemente alta, se produce una transferencia completa de electrones, dando lugar a la formación de especies iónicas.
Cuando se enlazan dos átomos iguales, con la misma electronegatividad, la diferencia es cero, y el enlace es covalente no polar, ya que los electrones son atraídos por igual por ambos átomos.
El criterio que se sigue para determinar el tipo de enlace a partir de la diferencia de electronegativad, en términos, generales es el siguiente:
ESTRUCTURA DE LEWIS
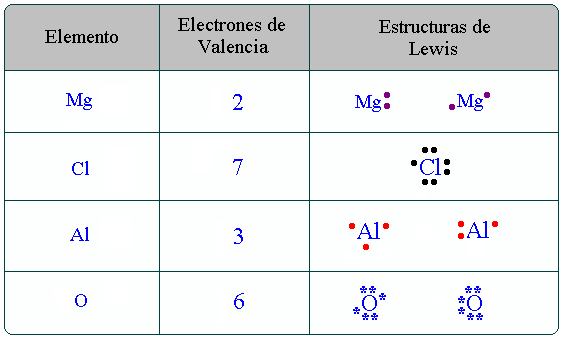
La estructura de lewis es una forma de representar los electrones de valencia de un átomo, es decir aquellos electrones que se encuentran en el último nivel energético de un átomo.
Para ello es necesario conocer el número atómico del elemento
y luego determinar la configuración electrónica.
Desde allí ubicar los electrones del último nivel.
Resumiendo:
Para hacer la estructura de lewis de un átomo debes:
1º.- conocer su número atómico (Z).
2º.- hacer su configuración electrónica.
3º.- desde allí sabrás los electrones del último nivel de energía.
4º.- ubicar los electrones alrededor del símbolo del elemento de acuerdo al siguiente esquema.
Para ello es necesario conocer el número atómico del elemento
y luego determinar la configuración electrónica.
Desde allí ubicar los electrones del último nivel.
Resumiendo:
Para hacer la estructura de lewis de un átomo debes:
1º.- conocer su número atómico (Z).
2º.- hacer su configuración electrónica.
3º.- desde allí sabrás los electrones del último nivel de energía.
4º.- ubicar los electrones alrededor del símbolo del elemento de acuerdo al siguiente esquema.
¿Cómo es la estructura de lewis del elemento nitrógeno? (Z= 7)
1º.- del número atómico (Z), podemos deducir que el número de electrones del nitrógeno es 7. (Átomo neutro).
2º.- su configuración electrónica es: 1s2-2s2-2p3.
3º.- podemos ver que en el segundo nivel de energía existen 5 electrones (2s2-2p3).
4º.- entonces siguiendo el esquema de lewis podemos escribir.
Con lo que la estructura de lewis quedará así
1º.- del número atómico (Z), podemos deducir que el número de electrones del nitrógeno es 7. (Átomo neutro).
2º.- su configuración electrónica es: 1s2-2s2-2p3.
3º.- podemos ver que en el segundo nivel de energía existen 5 electrones (2s2-2p3).
4º.- entonces siguiendo el esquema de lewis podemos escribir.
Con lo que la estructura de lewis quedará así
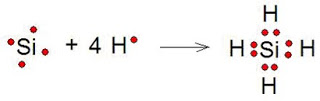
Todos los átomos tienden a tener ocho electrones en su último nivel ( según la llamada regla del octeto) a continuación una ecuación química que muestra la unión del silicio y cuatro átomos de hidrógeno.
Como puedes ver el silicio se encuentra estable debido a que en su último nivel de energía posee ocho electrones al igual que un gas noble.
Como puedes ver el silicio se encuentra estable debido a que en su último nivel de energía posee ocho electrones al igual que un gas noble.
ENLACE IONICO
Características:
- Esta formado por metal + no metal
- No forma moléculas verdaderas, existe como un agregado de aniones (iones negativos) y cationes (iones positivos).
- Los metales ceden electrones formando por cationes, los no metales aceptan electrones formando aniones.
- Son sólidos a temperatura ambiente, ninguno es un liquido o un gas.
- Son buenos conductores del calor y la electricidad.
- Tienen altos puntos de fusión y ebullición.
- Son solubles en solventes polares como el agua
ENLACES COVALENTES
Características:
FORMACIÓN DE ENLACES COVALENTES
Ejemplificaremos, con elementos que existen como moléculas diatómicas.
Cl2, cloro molecular, formado por dos átomos de cloro. Como es un no metal, sus átomos se unen por enlaces covalentes.
El cloro es un elemento del grupo VII A.
El átomo de cloro solo necesita un electrón para completar su octeto. Al unirse con otro átomo de cloro ambos comparten su electrón desapareado y se forma un enlace covalente sencillo entre ellos. Este enlace se representa mediante una linea entre los dos átomos.
Un enlace covalente sencillo, formado por dos electrones. Estos electrones se comparten por ambos átomos.
- Esta basado en la compartimento de electrones. Los átomos no ganan ni pierden electrones, COMPARTEN.
- Esta formado por elementos no metálicos. Pueden ser 2 o 3 no metales.
- Pueden estar unidos por enlaces sencillos, dobles o triples, dependiendo de los elementos que se unen.
- Los compuestos covalentes pueden presentarse en cualquier estado de la materia: solido, liquido o gaseoso.
- Son malos conductores del calor y la electricidad.
- Tienen punto de fusión y ebullición relativamente bajos.
- Son solubles en solventes polares como benceno, tetracloruro de carbono, etc., e insolubles en solventes polares como el agua.
FORMACIÓN DE ENLACES COVALENTES
Ejemplificaremos, con elementos que existen como moléculas diatómicas.
Cl2, cloro molecular, formado por dos átomos de cloro. Como es un no metal, sus átomos se unen por enlaces covalentes.
El cloro es un elemento del grupo VII A.
El átomo de cloro solo necesita un electrón para completar su octeto. Al unirse con otro átomo de cloro ambos comparten su electrón desapareado y se forma un enlace covalente sencillo entre ellos. Este enlace se representa mediante una linea entre los dos átomos.
Un enlace covalente sencillo, formado por dos electrones. Estos electrones se comparten por ambos átomos.
Enlace covalente coordinado:
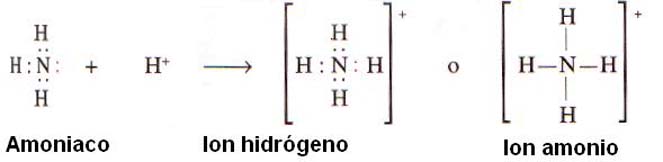
Se forma cuando el par electrónico compartido es puesto por el mismo átomo. Ejemplo:
Se forma cuando el par electrónico compartido es puesto por el mismo átomo. Ejemplo:
En el siguiente link encontraras mas información de los enlaces químicos:
ENLACES ENTRE ÁTOMOS
ENLACES ENTRE ÁTOMOS